来源 :键凯科技PEGylation2024-02-06

键凯科技(688356.SH)
SM-102获DMF备案


SM-102是一种可电离的氨基脂质,与其他脂质结合用于形成脂质纳米颗粒。
SM-102 CDE公示信息如下:
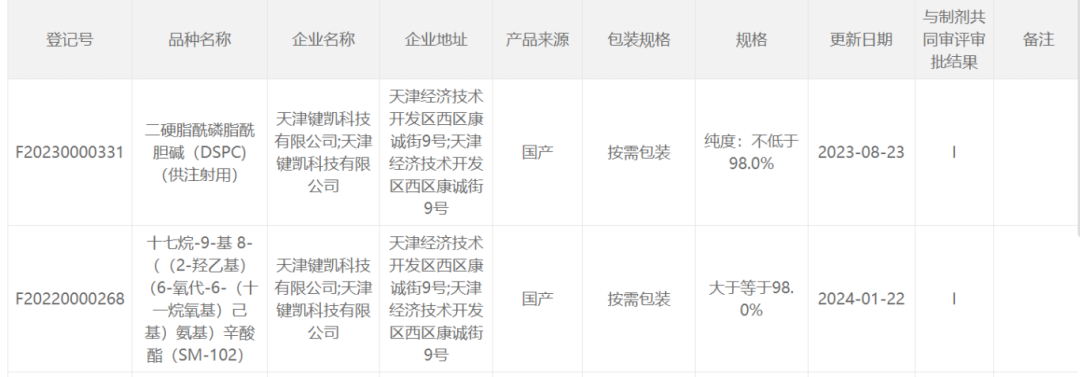
未来,使用键凯科技该产品的药物申报者可以直接使用键凯的DMF备案编号进行关联申报,可极大程度上缩短评估和申报时间。
JenKem

键凯科技专业的合成开发部门,分析方法开发部门、质量研究部门和各种PEG衍生物生产线,可满足您从辅料合成筛选,GMP生产和药用辅料登记等对新型脂质开发的全流程需求。
职能体系
美国生物制品的监管主要由美国食品药品监督管理局(FDA)的药物评价和研究中心(CDER)和生物制品评价与研究中心(CBER)负责。CDER监管的生物制品一般是治疗用蛋白制剂,CBER监管的产品包括细胞及基因治疗产品、血液制品以及疫苗。
DMF-药品主文件
药品主文件(DMF, Drug Master File)是向美国食品药品管理局(FDA)提交的文件,可用于提供一种或多种人类药物制造、加工、包装和储存过程中使用的设施、工艺或物品的机密详细信息。DMF中包含的信息可用于支持研究新药申请(IND)、新药申请(NDA)、缩写新药申请(ANDA)、另一DMF、出口申请或对这些申请的修订和补充。
DMF的类型
I类:制造场地、设施、操作程序和人员
II类:原料药、原料药中间体及其制备材料或药品
III类:包装材料
IV类:辅料、着色剂、香料、香精或用于其制备的材料
V类:FDA接受的参考信息
键凯科技在FDA已备案15个品种,CDE备案5个品种。公司可稳定持续生产高质量产品并正在持续办理更多组分的DMF申报工作。
键凯热线:010-82156767
键凯销售:010-62983737
电子邮箱:sales@jenkem.com
扫码关注
键凯科技
(688356.SH)