报告摘要
百济神州的CDK4抑制剂BGB-43395进度处于前列,有望成为全球第二款进入注册临床阶段的CDK4抑制剂
根据公司指引,BGB-43395预计在未来的6-12个月内进入注册临床阶段。BGB-43395目前开展了3项I期临床,试验方案涵盖了单药或联合内分泌疗法(ET,EndocrineTherapy)二线治疗,以及联合ET和BCL2i三线治疗HR+/HER2-BC。
CDK4抑制剂BGB-43395在多个体内外药效评估中均展现出BIC潜力
BGB-43395相较现有CDK4/6抑制剂具有更高选择性。BGB-43395在GLP毒理研究中表现良好,未见显著中性粒细胞减少或胃肠道毒性。百济神州的BGB-43395体内药代动力学数据符合预期,药效学活性强效。
CDK4抑制剂BGB-43395具有更优抑制效力。目前CDK4i领域FIC的药物是进入III期临床的辉瑞的PF-07220060,在MCF-7增殖实验中,BGB-43395的抑制细胞增殖效力IC??为126nM,比PF-07220060更强(后者为544nM),活性提升4.3倍,展现出卓越疗效。
后续随访时间延长,整体响应率有望大幅提升
从辉瑞披露的数据可以看到,CDK4抑制剂Atirmociclib的中位起效时间是3.6M。所以对同靶点药物,百济神州的CDK4i来说,3个月的中位随访时间还未到中位起效时间。过往数据提示CDK4/6i的应答率随时间延长逐步提升,在9个月时达到最高应答概率。BGB-43395在3个月的评估时间看到240mg、400mg、600mgBID联用组SD+PR为67%(8/12),83%(5/6),75%(6/8),趋势较好。
目录

正文
1. BGB-43395 跻身新一代高选择性CDK4抑制剂研发前列
新一代CDK抑制剂赛道大部分在研品种处于I/II期临床阶段,仅有辉瑞制药的Atirmociclib推进至III期临床阶段。根据insight数据库显示,目前在CDK4i领域,共有四款药物进入临床试验阶段,其中进度最为领先的是辉瑞的Atirmociclib(PF-07220060),HR+/HER2-BC的一线和二线治疗均已进入III期临床试验。
百济神州的BGB-43395进度处于前列,有望成为第二款进入注册临床阶段的同靶点药物。根据公司指引,BGB-43395预计在未来的6-12个月内进入注册临床阶段。BGB-43395目前开展了3项I期临床,试验方案涵盖了单药或联合内分泌疗法( ET ,EndocrineTherapy)二线治疗,以及联合ET和BCL2i三线治疗HR+/HER2-BC。根据指引,BGB-43395最早能于今年启动2LBC 的III期全球多中心临床试验,有望成为第二款进入注册临床阶段的药物。

2. CDK4抑制剂BGB-43395相较FICCDK4i显示出更强的选择性和抑制效力
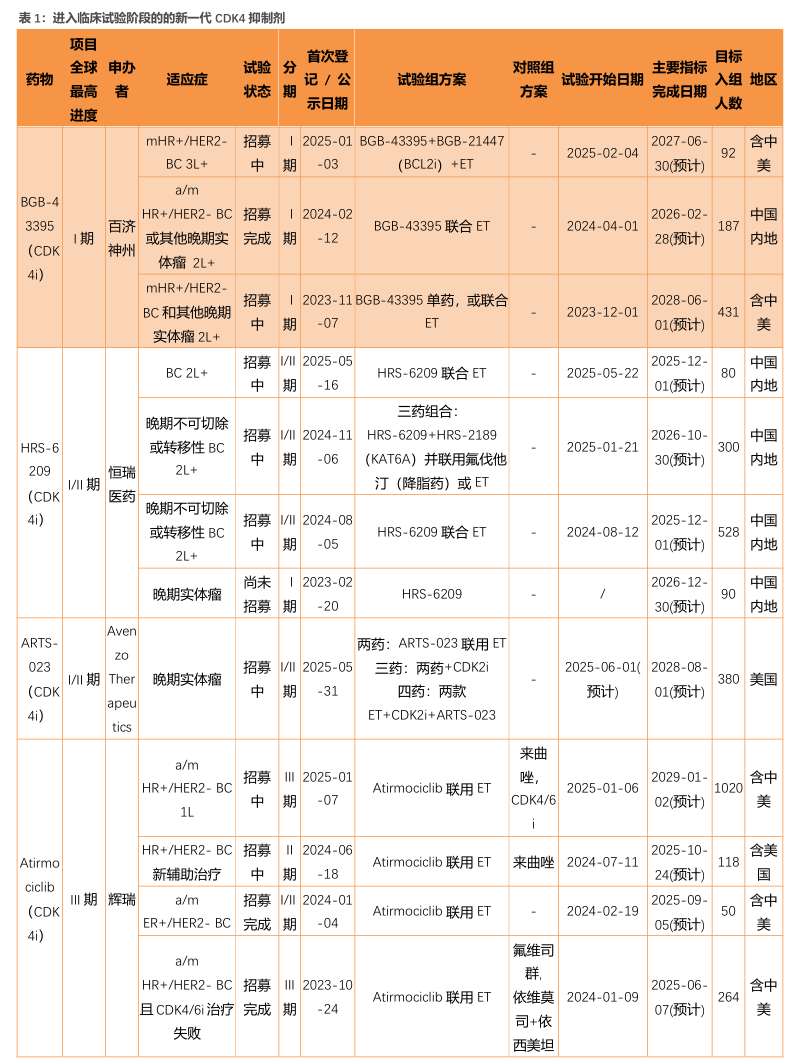
BGB-43395 相较现有CDK4/6抑制剂具有更高选择性。CDK4/6抑制剂在HR+/HER2-乳腺癌领域商业成功,全球销售峰值预计超180亿美元;根据IQVIAMIDAS?的数据,2024年全球CDK4/6i 抑制剂市场销售额为147.77亿美元,同比增长17%。已有3款FDA批准药物,但均存在毒性问题。而BGB-43395(CDK4i)选择性抑制CDK4,CDK6/CDK4IC??比值高达38倍,远高于其他产品(PF-07220060: 21;Abemaciclib: 16;Ribociclib: 7.7;Palbociclib: 1.3),说明几乎不抑制 CDK6,选择性非常好,可避免CDK6介导的毒性及其它脱靶毒性,安全性更优。BGB-43395在GLP毒理研究中表现良好,未见显著中性粒细胞减少或胃肠道毒性。
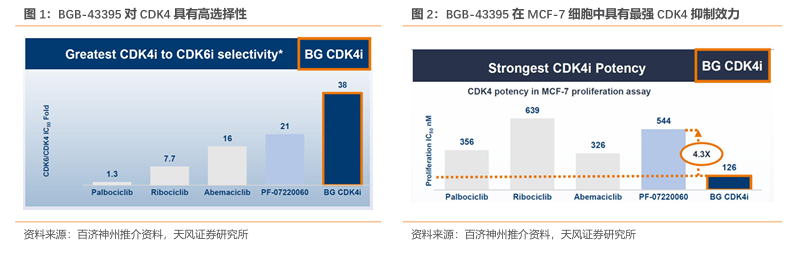
BGB-43395 具有更优抑制效力。目前CDK4i领域FIC的药物是进入III期临床的辉瑞的PF-07220060,在 MCF-7 增殖实验中,BGB-43395的抑制细胞增殖效力IC??为126nM,比PF-07220060 更强(后者为544nM),活性提升4.3倍,展现出卓越疗效。
3. CDK4抑制剂BGB-43395体内数据亮眼,药代动力学和药效学数据符合预期
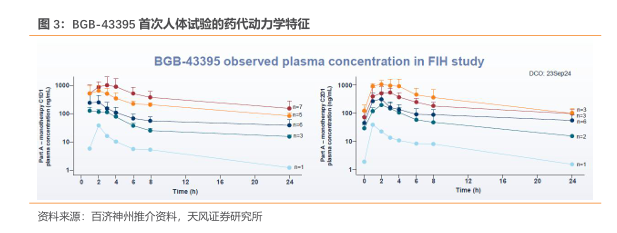
CDK4抑制剂BGB-43395在测试的剂量水平中显示出预期的药代动力学特征。BGB-43395单药在与CDK4依赖相关的晚期实体瘤患者中的初步临床数据显示,其口服后快速吸收,Tmax 中位数约为2小时。半衰期约为13小时。暴露水平与剂量呈比例增加。与 fulvestrant或 letrozole 联合用药不影响暴露水平。
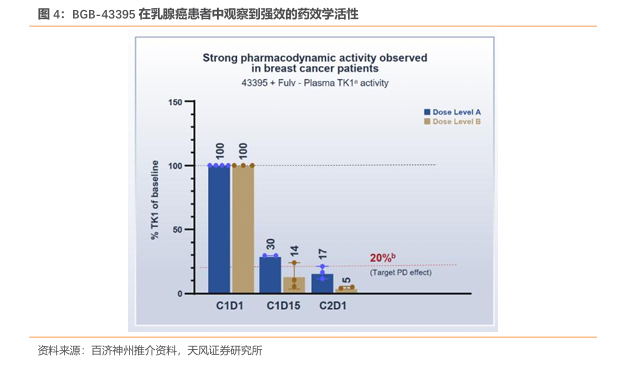
BGB-43395 药效学效应强,达到目标水平。 BGB-43395与氟维司群联合治疗的剂量A和剂量B对患者血液中TK1抑制水平达到了目标药效学效应。TK1是DNA合成补救途径的关键酶,负责催化胸苷磷酸化为胸苷一磷酸(dTMP),为DNA复制提供原料。在细胞周期中,TK1活性在G1/S期显著升高,直接驱动细胞进入DNA合成阶段。乳腺癌等恶性肿瘤细胞因异常增殖,TK1表达水平远高于正常组织(可达健康人的2-5倍)。这一指标直接反映药物对肿瘤细胞DNA合成能力的抑制效果,是评估治疗响应的重要生物标志物。
4.参照同类CDK4i起效时间,CDK4抑制剂BGB-43395疗效潜力显著
辉瑞披露的数据可以看到,CDK4抑制剂Atirmociclib的中位起效时间是3.6M。所以对同靶点药物,百济神州的CDK4i来说,3M的中位随访时间还未到中位起效时间。
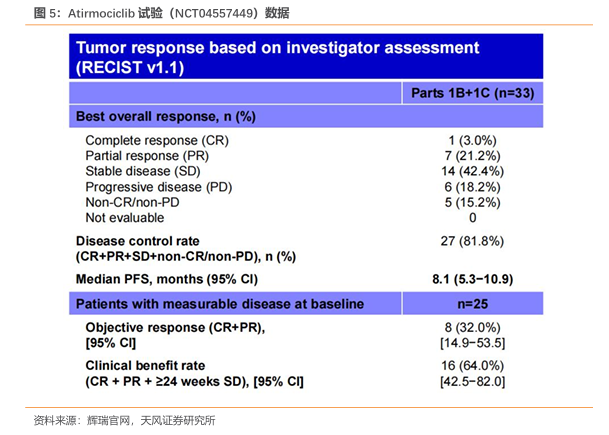
同时,从辉瑞的蜘蛛图数据中也可以看到该类分子后续的疗效是持续性强的,ORR为32%,CBR 为64%。
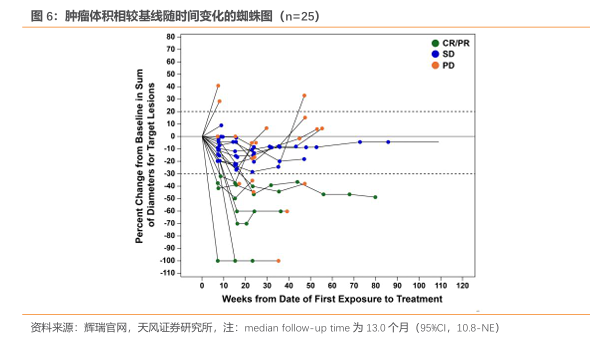
5.参照CDK4/6i响应率时间,CDK4抑制剂BGB-43395后续响应率有望提升
在MONARCH试验中,对阿贝西利的响应在接近9个月的时候达到。阿贝西利组在随机分组后3个月有一批患者治疗起效,在大约 9 个月时达到最大反应概率;阿贝西利组的最大反应概率为 53.4%。
根据阿贝西利的结果也可以合理推测,BGB-43395的3个月的中位观察期较短,后续随治疗时间延长,患者响应率有望有比较大的提升。
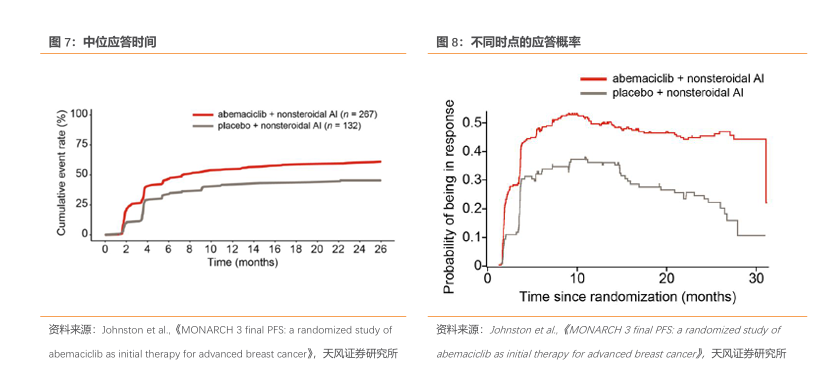
6. CDK4抑制剂BGB-43395早期临床数据初显较优抗肿瘤响应率
BGB-43395 在 3 个月的评估时间看到 240mg、400mg、600mg BID 联用组 SD+PR 为67%(8/12),83%(5/6),75%(6/8),趋势较好。我们认为后续随访时间延长,整体响应率有望大幅提升。
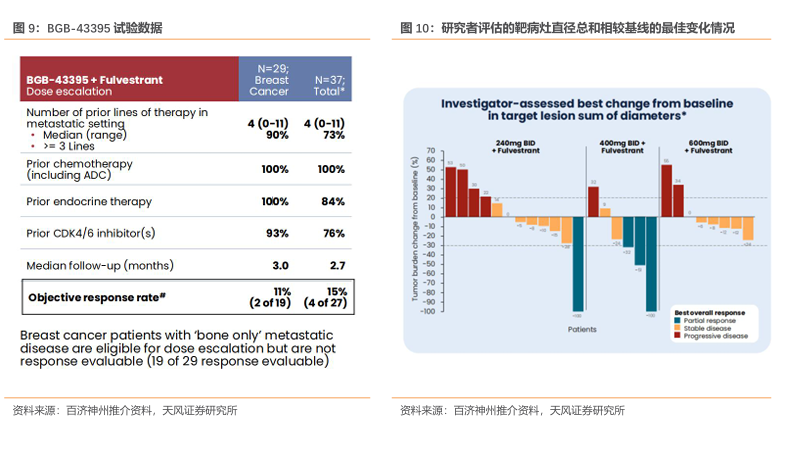
风险提示
公司产品商业化进度不及预期风险、政策变动风险、研发进展不及预期风险、核心技术人员流失风险、市场竞争加剧风险