来源 :NOVOPROTEIN2023-11-17
2023年11月16日(当地时间),Vertex Pharmaceuticals和CRISPR Therapeutics共同宣布,体外基因编辑疗法Exagamglogene Autotemcel(Exa-cel,CASGEVY?)获得英国药品监管机构MHRA有条件批准上市,用于治疗镰状细胞病(SCD)和输血依赖性β-地中海贫血(TDT),这是全球首款获批上市的CRISPR基因编辑疗法(Cas9蛋白与sgRNA体外电转至患者离体细胞,编辑后的细胞回输患者体内)。
近岸蛋白GMP级Cas9蛋白助力基因编辑疗法开发
近岸蛋白基于成熟的技术平台和严格的质量管理体系,提供GMP级Cas9蛋白,助力基因编辑疗法开发。
CASGEVY?是一种一次性单剂量细胞基因治疗药物,由经过CRISPR/Cas9介导的基因编辑的自体CD34+人类造血干细胞和祖细胞(hHSPC)组成,Cas9蛋白与sgRNA在体外经电穿孔的方式被递送到患者的离体细胞内,RNP复合体会结合在位于BCL11A基因内含子上的红细胞特异性增强子中――转录因子GATA1的结合区域,在引入双键断裂(DSB)后,利用非同源末端连接修复(NHEJ)产生突变,破坏该增强子,降低BCL11A在红细胞中的转录水平,从而特异性提高胎儿血红蛋白(HbF)在红细胞中的表达,HbF水平的升高能够缓解或消除SCD患者的疼痛及血管闭塞性危象(VOC),并且能缓解TDT患者的输血需求,使TDT患者摆脱长期输血的困扰。
 来源:https://www.sec.gov/Archives/edgar/data/1674416/000156459020056242/crsp-ex992_7.htm
来源:https://www.sec.gov/Archives/edgar/data/1674416/000156459020056242/crsp-ex992_7.htm
针对CD34+hHSPC基因组的编辑过程仅在离体状态中短暂进行,因此当CASGEVY?细胞回输给患者时,细胞中不存在残留的基因编辑活性。
 来源:CRISPR Therapeutics
来源:CRISPR Therapeutics
在Vertex和CRISPR Therapeutics公布的一项针对SCD治疗临床试验中,45名SCD患者接受了CASGEVY?的治疗,其中的29名患者达到了至少18个月的随访,这29人中的28人在治疗后至少一年内没有疾病相关的严重疼痛症状出现。在一项针对TDT的临床研究中,迄今为止已有54名患者接受了CASGEVY?的治疗。在随访时间足够长的42例患者中,有39例患者在治疗后至少一年内不需要输血,其余3人的输血需求减少了70%以上。
目前CASGEVY?在英国的定价还没有确定,此前有分析师预测其定价将大于200万美元。在美国,该款药物治疗SCD适应症预计也将在2023年12月8日获批上市,治疗TDT预计将在2024年3月30日获批上市。
Recombinant Cas9 Nuclease, GMP Grade
(目录号:GMP-1701)
GMP级Cas9蛋白(进口品质,国产价格)


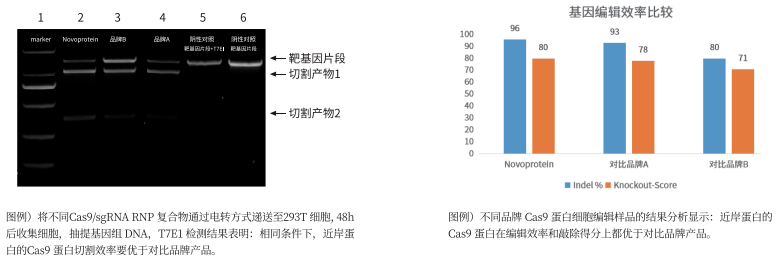
基因编辑效率高
基因编辑相关产品
| 目录号 |
产品名称 |
| GMP-1701 |
Recombinant Cas9 Nuclease, GMP Grade |
| E365 |
NLS-Cas9 Nuclease |
| E369 |
sgRNA In Vitro Transcription Kit |
| E370 |
sgRNA Screening and Genotype Confirmation Kit |
| E366 |
Cas9(D10A) Nickase |
| E367 |
Cas9(H840A) Nickase |
| E368 |
Cas9(D10A, H840A) Nuclease |
| E379 |
NLS-Cas9-EGFP Nuclease |
| E373 |
LbaCas12a Nuclease |
| E381 |
LwaCas13a Nuclease |
| M017 |
T7 Endonuclease I |
| MR107 |
Cas9 mRNA |
| MR019 |
Cas9 mRNA (N1-Me-Pseudo UTP) |
| GMP-MR005 |
piggyBac mRNA, GMP Grade |
近岸蛋白还提供符合临床申报要求的GMP级细胞因子,高纯度,高活性,高批间一致性,低内毒(<10EU/mg),助力CD34+ HSC培养。