投资要点
| 投资要点 GC001为心梗治疗领域FIC,全球重磅大单品潜力。杜吉普单抗(SGC001)已获中美IND批件,并于25M3获FDA授予的快速通道认证,有潜力成为全球首款心肌梗死(AMI)治疗抗体药物。且临床前疗效理想,在全梗恒河猴模型中,SGC001分别低、中、高剂量下单次静脉给药可显著增加心梗恒河猴的心脏血流供应,并减轻心肌组织病变程度,其中降低心肌梗死体积均值分别减少23%、43%、53%,改善心功能射血分数分别提升了55%、141%、175%,具有优良的成药特性。临床Ib期临床已完成,有望近期披露主要数据,有出海BD潜力。积极布局创新管线,多家子公司打开创新成长新空间。公司在肿瘤、神经、心血管领域均有靶点发现和管线产出。子公司尧景基因和舜景医药除心血管领域重磅分子SGC001外,还有肝外靶向小核酸平台和肿瘤领域靶向Tregs细胞的双抗药物SGT003。参股公司智源生物在神经系统领域拥有靶向Aβ蛋白的单抗药物AA001。公司创新抗体产品均使用独家发现的最新靶点,和市场上其余产品形成差异化,在同赛道药物中规避了机制同质化的竞争。 IVD业务贡献基本盘,产品布局全面,前沿技术平台领先。公司在体外诊断领域,一方面继续扩展磁微粒化学发光、上转发光等原有技术开发;另一方面积极拓展基于国际领先糖捕获技术的“国人肝健康工程”、“国人脑健康工程”和“国人癌症早诊早筛工程”为核心技术的三大“国人健康工程”,进一步拓宽体外诊断领域的核心战略布局;经过多年发展,构建了噬菌体大容量全合成人抗体制备技术平台、糖捕获技术平台、磁微粒化学发光技术平台、上转发光技术平台等多项核心技术平台,拥有多项前沿创新技术和创新产品,开发了一系列的体外诊断试剂及仪器,可应用于全场景的免疫诊断。盈利预测与投资评级:我们预计公司2025-2027年实现收入5.42/5.97/6.67亿元,实现归母净利润-1.22/-0.14/0.16亿元。主业IVD、创新药及小核酸平台合计有望贡献480亿市值。考虑公司主业IVD业务贡献基本盘,参股公司创新药管线持续推进,核心产品SGC001为AMI领域FIC,逐步转型创新,首次覆盖,给予“买入”评级。风险提示:产品研发失败风险;销售不及预期风险;集采风险。 |


1. 热景生物:深耕IVD,创新药打开增长空间
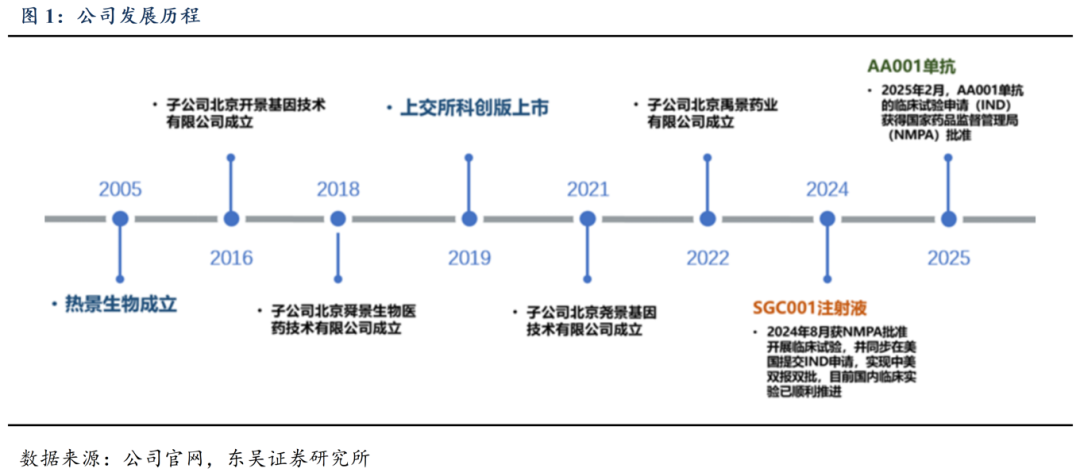
热景生物创立于2005年,2019年在上海证券交易所科创板上市。公司不断探索自主创新诊断技术平台,通过参股开景基因、尧景基因、舜景医药、禹景药业等子公司,分别布局核酸药物、抗体药物、新型益生菌等生物制药创新领域,建立了包括蛋白标志物糖链外泌体、DNA甲基化等多组学诊断技术平台。旗下创新技术孵育平台未来技术研究院现已布局核酸药物、抗体药物及生物技术消费品等前沿领域,全球首款心梗抗体药物已进入中美临床研究,SGC001注射液用于急性心肌梗死(AMI)患者的急救治疗。
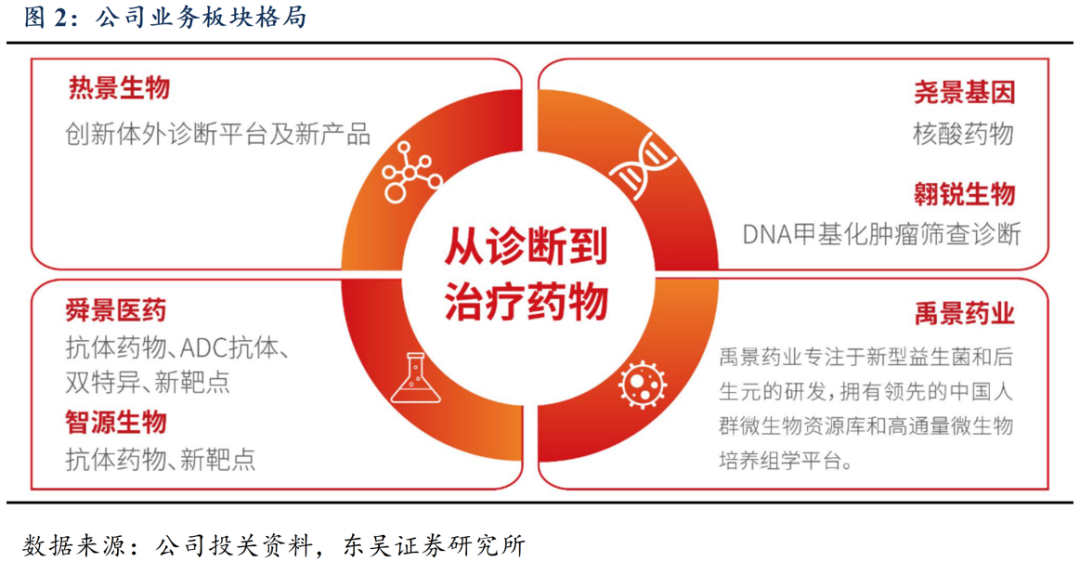
业务板块多样,参股公司及子公司分工明确。热景生物深耕体外诊断产品领域,依托多项前沿技术平台构建了全面的产品矩阵。公司成立子公司和联营企业包括:尧景基因、舜景医药、禹景药业等,拓展从诊断到治疗药物的全治疗链路。
管理层研发能力强,研发成果屡获荣誉。公司董事长林长青先生曾在万泰药业拥有20年行业技术经验,深耕传染病诊断领域,带领团队研制了近百种创新型诊断试剂。所获专利20余项,主持863项目子课题2项、重大传染病专项子课题1项、中小企业创新基金项目2项,北京市科委成果转化等项目4项,在IVD领域成果丰富,荣获国家技术发明奖二等奖、国家科技进步二等奖、全国抗击新冠肺炎疫情先进个人、首都劳动奖章等20余项奖项。其他高管成员均具备深厚的专业背景和卓越的科研能力,在创新药研发、体外诊断技术突破等方面成果显著。

股权结构稳定,子公司布局全面。董事长林长青为实控人,直接持有公司23.45%股权,并通过青岛同程间接持有公司0.96%的股权。董事周锌持有7.36%的股份。其他股东包括同程热景、浙江大健康投资及个人股东邵魁、陈建辉、孙守用等。子公司方面,公司拥有廊坊热景、深圳热景、香港热景、美国热景、热景检验、开景基因100%股权、印度热景99%股权、禹景药业52%股权。在重要联营企业中,热景生物持有舜景医药和尧景基因各48%的股份,朝锐生物35.81%的股份,以及智源生物21.58%的股份。公司通过持股旗下“尧、舜、禹”子公司,布局小核酸药物、抗体药物、微生物等医药领域。
通过持股计划绑定核心员工。2024年5月,公司发布2024年员工持股计划,拟以14.63元/股的价格受让公司回购股份的数量不超过2,861,477股,占公司股本总额3.09%。参加本员工持股计划的员工总人数不超过142人,其中参加本员工持股计划的董事(不含独立董事)、监事和高级管理人员共计9人。未来公司将继续推进股权激励计划,以激励核心员工,提升长期竞争力和创新能力。
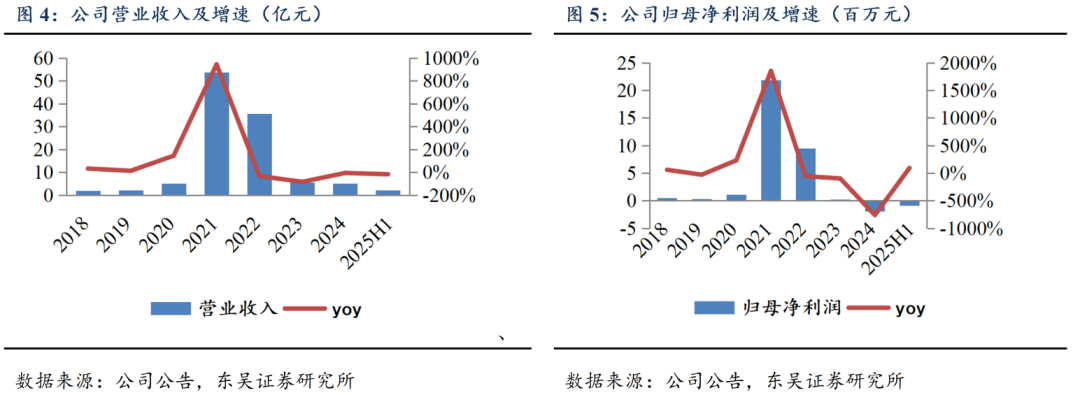
营收及归母净利润概览:公司2021年因新冠抗原检测试剂盒的海外收入放量导致业绩高增长,疫后需求回落,对营收、净利润影响出清。公司逐渐回归传统检测业务模式,2024年实现营业收入5.11亿元,同比下降6.74%,相比2023年扣除非常规检测业务后同比增长23.10%。
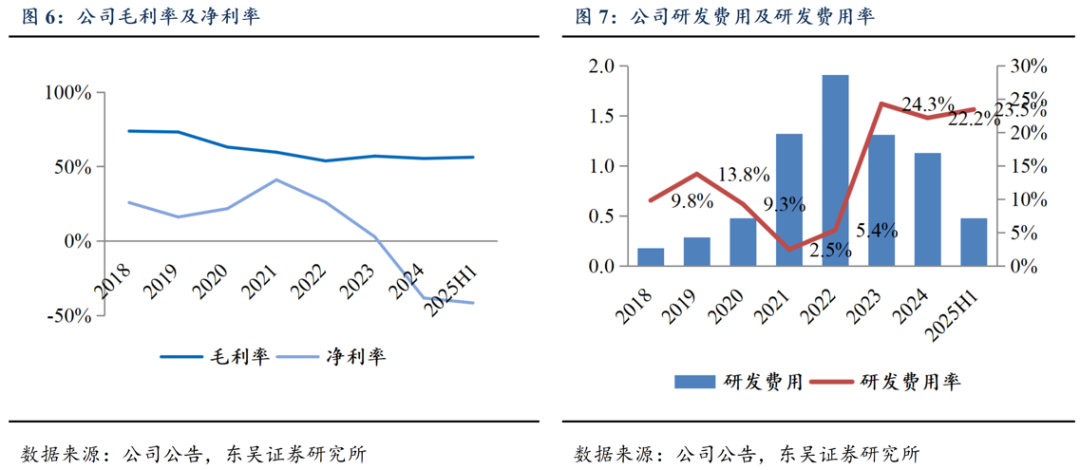
加大研发投入,创新药打开增长空间。公司疫后仍保持较高研发投入,2024年为1.13亿元,对应研发费用率为2024年研发投入为1.13亿元,同比减少0.18亿元。研发费用率为22.18%,较2022年以前大幅提升。公司未来将持续布局创新药领域,针对核心产品SGC001、AA001等开展临床,打开增长空间。
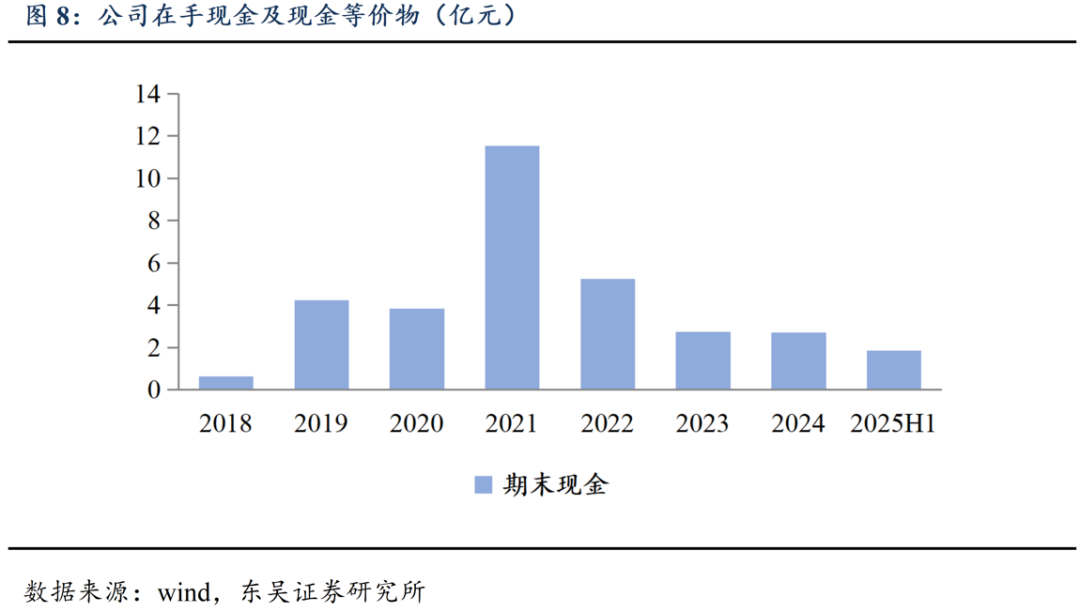
在手现金充足。公司2024年末持有现金及现金等价物2.70亿元,2025H1末持有现金1.84亿元,流动资产合计13.37亿元。自2021年非常规检测业务显著放量后,公司将红利期收入转化为研发成果,通过创新药管线驱动公司进一步发展转型,实现长期战略。我们认为公司目前账面现金及现金等价物足够支持公司后续研发工作及业务开展。
2. 全面布局创新药,SGC001具备大单品潜力
公司通过参股公司舜景医药、尧景基因、智源生物等创新药企,构建差异化创新药管线,聚焦抗体药物与核酸药物两大核心技术领域。从单一体外诊断领域向创新药迈进。疾病聚焦在心脑血管领域,拓展至肿瘤、神经退行性疾病和代谢性疾病等。

2.1. 舜景医药:SGC001为心梗治疗领域FIC
公司重要参股公司舜景医药由孙志伟研发团队发起,负责公司抗体药物研发板块的拓展。其核心产品杜吉普单抗(SGC001)是一款针对急性心肌梗死(AMI)进行急救治疗的单克隆抗体。目前SGC001注射液已获得中美IND双报双批认证,成为全球首款心肌梗死治疗抗体药物。
2.1.1. AMI市场空间大,亟需药物开发
AMI发病急、病情重、死亡率高。急性心肌梗死(AMI)是由于冠状动脉突然完全或几乎完全阻塞,导致心肌细胞缺血缺氧并发生坏死的急性心血管疾病,属于急性冠脉综合征(ACS)的严重类型,AMI根据心电图改变和心肌损伤标志物的有无及类型分为ST段抬高型心肌梗死和非ST段抬高型心肌梗死。AMI典型症状包括持续剧烈胸痛(常放射至左臂或下颌)、呼吸困难、出汗、恶心等,若不及时治疗,可能引发心力衰竭、心律失常甚至猝死,每年导致全球约300万人死亡,中国约250万人死亡。
据国家心血管病中心《中国心血管健康与疾病报告2023》的数据,AMI在中国的死亡率,农村为83.26/10万,城市为63.25/10万,更严重的是AMI愈后1年内高达的48%患者再次住院,其中57%诊断为主要心血管不良事件(MACE)。
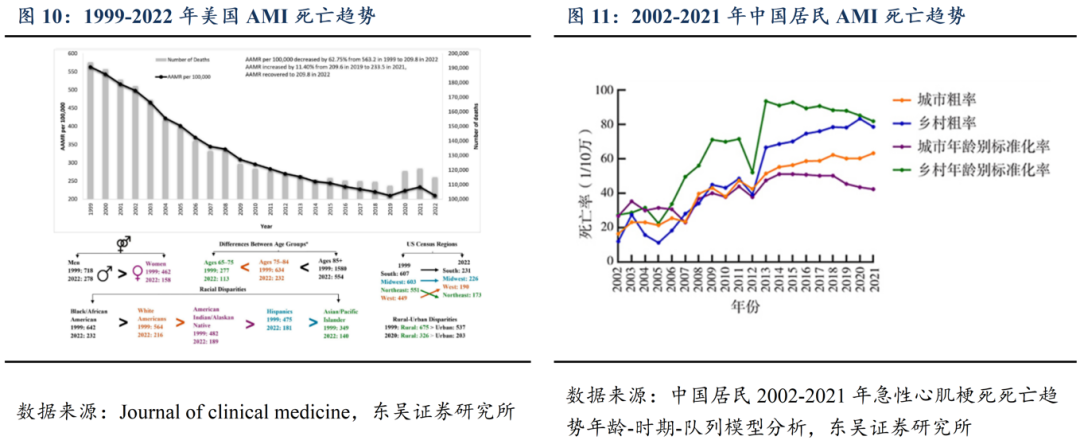
AMI患者基数大,每年新发患者众多。流行病学研究显示,全球60岁以下和60岁以上人群的AMI患病率分别为3.8%和9.5%。2022年报告指出,我国存量冠心病人群1139万人,报告预计2030年可达2300万人。近年来得益于冠脉支架置入,药物溶栓等治疗方式的进步和胸痛急诊绿色通道的建设,AMI的死亡率有所下降,但随着社会经济的快速发展,年轻群体生活方式改变,AMI发病率呈年轻化趋势。
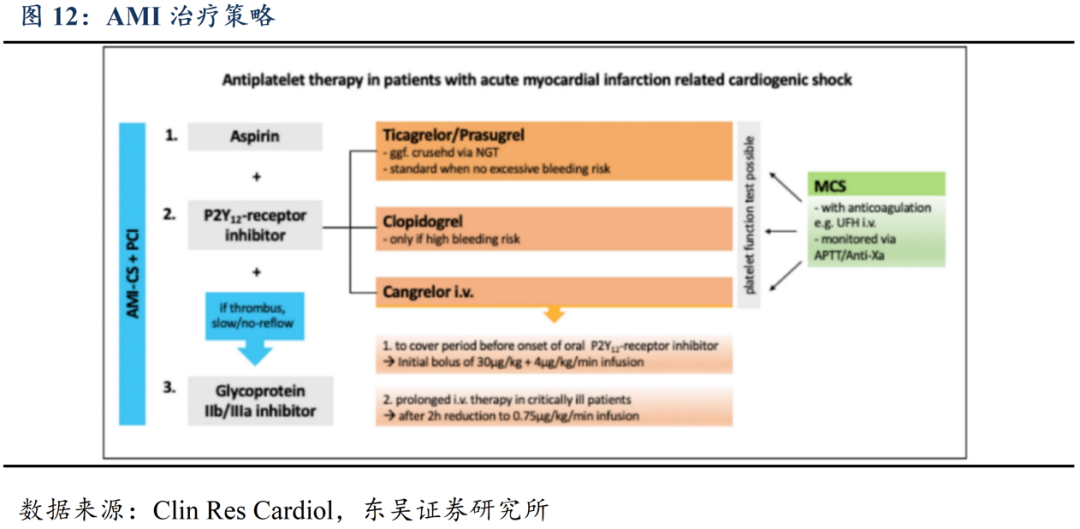
AMI治疗手段匮乏,药物治疗市场待开发。AMI的常规治疗手段主要分为再灌注治疗和药物治疗。再灌注治疗包括药物溶栓、PCI及冠状动脉旁路移植术,通过尽快恢复心肌有效再灌注,缩小梗死面积,以降低发病率和死亡率。药物治疗包括抗血小板药、降脂药物、β-受体阻滞剂、血管紧张素转换酶抑制剂、血管紧张素受体脑啡肽酶抑制剂等,可抑制AMI后心室重塑,改善心脏功能,维持血液动力学稳定。目前,全球范围内还没有针对降低炎症通路,减少心肌细胞损伤的抗炎新机制药物上市。
当前临床上对AMI的治疗思路主要以恢复血供并降低心负荷为主。其中主要针对心肌梗死的药物治疗方法包括溶血栓治疗、抗凝疗法、β受体阻滞剂、钙拮抗剂、极化液和激素等。但无论是药物疗法还是搭桥、球囊扩张、支架置入等外科疗法均无法挽救已坏死的心肌细胞,会无可避免导致心功能下降,从而导致后续心脏重构和炎症反应发生,致使后续心衰及其他并发症的发生,新型急性心肌梗死药物亟待开发。
此外,随着AMI再灌注治疗的普及,心梗后心肌炎症反应相关心衰人群大幅增加。而现有药物疗法用药基本只有降压、抗凝类药物,无法对心肌细胞的炎症性损伤进行保护,严重紧缺相关创新药,有较大未被满足的临床需求。因此为了提高AMI的临床疗效,亟需探索能改善心肌再灌注损伤和缺血后炎症反应的创新药物及其机制。
长期反复的无菌性炎症是AMI发生发展的重要致病机制。AMI致病机制分为心肌纤维化、心肌炎症、血管阻塞等病理反应。其中长期反复无菌性炎症是心肌纤维化的基本病理机制,后续成纤维细胞的增殖和表皮转化可以导致心衰,心脏室壁瘤乃至心脏破裂、死亡等后果。严重缺血缺氧情况下局部炎症反应在AMI初期迅速激活,中性粒细胞和单核细胞被招募至缺血区域,并释放炎症介质,刺激受损组织促炎症反应。
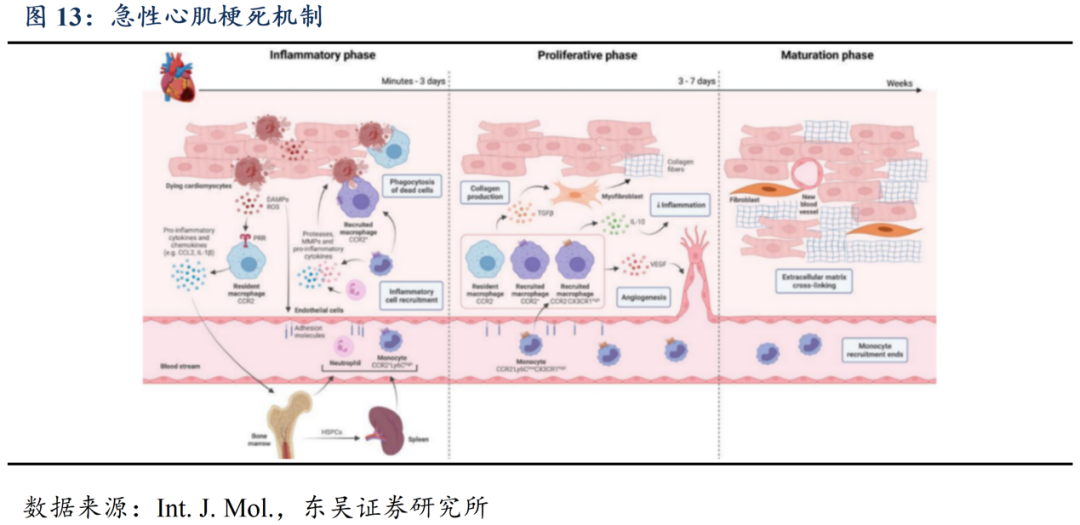
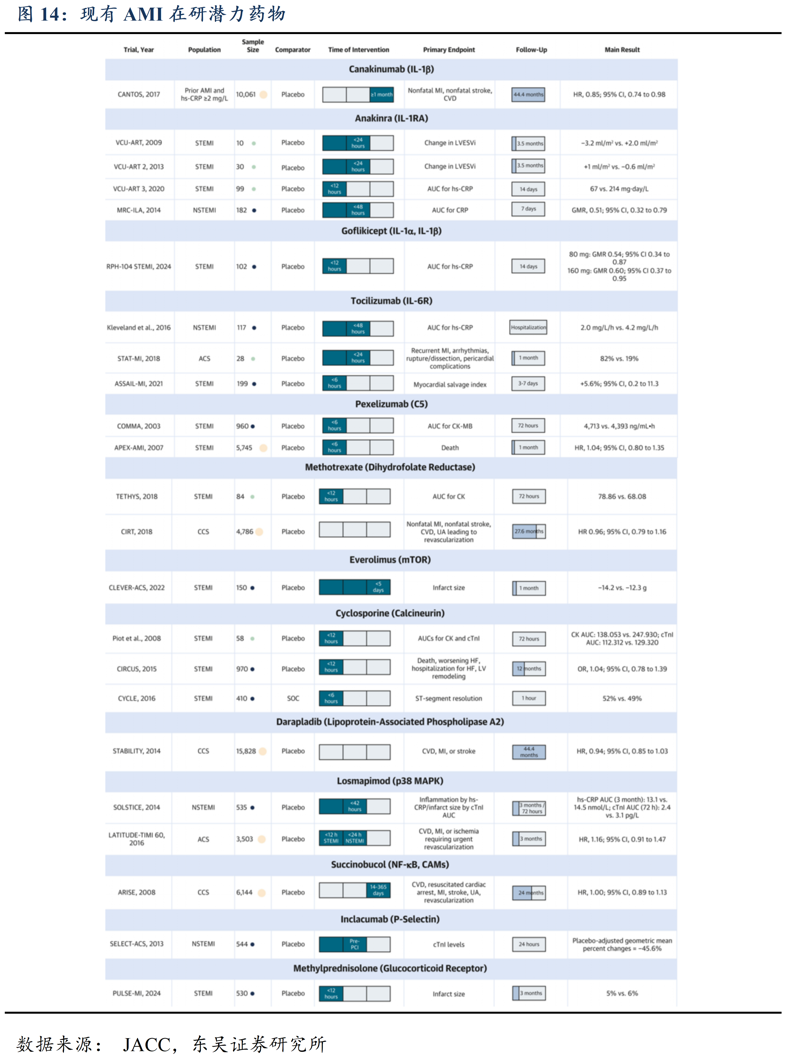
AMI发生后级联反应诱发过度炎症的关键介质是NLRP3炎症小体,它通过激活caspase-1 来响应胆固醇晶体、氧化等应激源,激活IL-1β作为促进内皮活化、白细胞募集和细胞因子产生,激活IL-18诱导干扰素-γ产生促进巨噬细胞活化和T细胞应答,激活IL-6导致血管功能障碍和心肌异常重塑。而产生的炎症反应进一步扩大AMI造成的心肌损害,导致更多斑块破裂,加速梗死灶形成。目前对AMI的炎症通路相关治疗药物仍着眼于已被发现的传统靶点,主要包括:减弱嗜中性粒细胞活化的微管蛋白聚合抑制剂,如秋水仙素;靶向 IL-1 途径的药物阻断 IL-1 信号传导以减少下游炎症级联,如卡那单抗、阿那白滞素、Goflikicept;靶向IL-6途径的调控全身免疫效应的Ziltivekimab、Tocilizumab、Pacibekitug;其他经典免疫抑制剂,如环孢素、甲氨蝶呤等。
现有的AMI相关免疫治疗存在下游靶点作用有限,上游靶点靶向性差导致副反应严重的问题。LoDoCo2、COLCOT、CLEAR等大型临床试验提示针对秋水仙素/IL-1β/免疫抑制剂等全身作用的炎症靶点在AMI中存在安全风险,未必能为患者带来获益。目前指南中,仅推荐去秋水仙素作为AMI疾病的预防用药(欧洲ESC/美国CCS,2a级推荐),尚无用于AMI发生后的免疫疗法。多数AMI免疫疗法处于临床阶段,且甲氨蝶呤等传统药物表现不理想未继续推进后期临床和适应症拓展。靶向IL-6的诺和诺德拥有的Ziltivekimab为AMI炎症通路药物的实质FIC分子,紧随其后的是Tourmaline拥有的Pacibekitug,同为IL-6药物。
2.1.2. IL-6药物领衔炎症疗法赛道,临床评估方式局限
由于目前人们对AMI发生后炎症损伤机制认知有限,目前对缺乏经过验证的生物标志物和临床指标,无法可靠地识别最有可能从抗炎治疗中受益的患者。故心衰领域新药研发的终点指标往往多样化,非关键临床指标缺乏可比性。
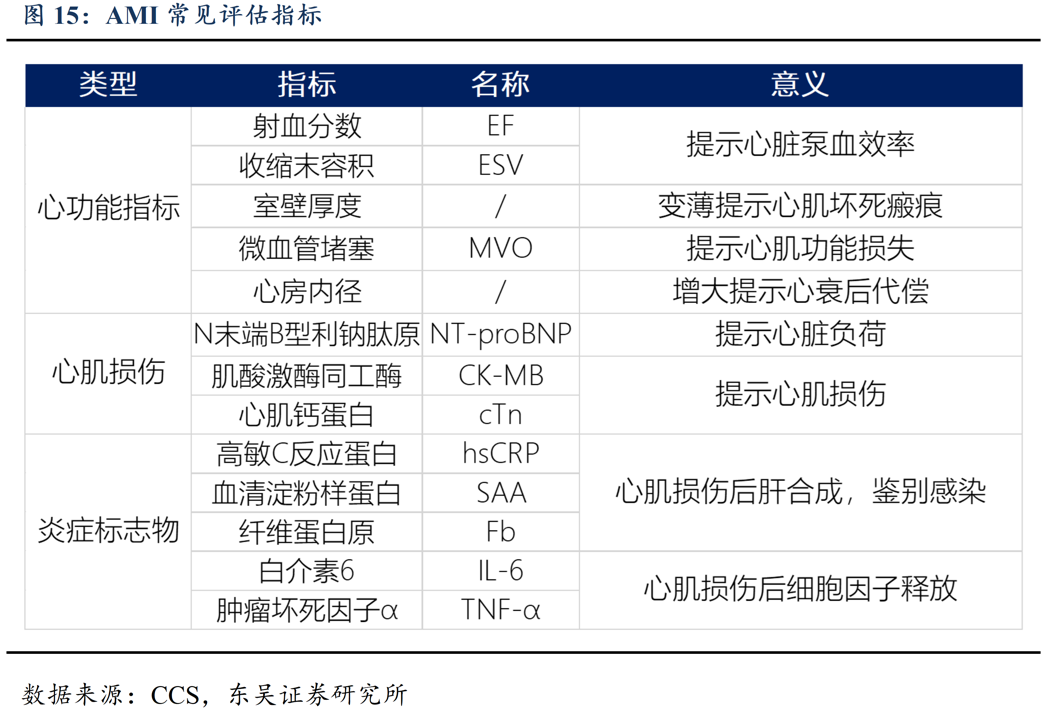
对AMI心脏功能影响的分析手段包括射血分数、心房内径、室壁厚度、MVO(微血管堵塞)心肌等超声下功能评估指标。AMI后患者常因心肌损伤导致收缩泵血能力不足,出现心功能下降,心肌损失的表现。室壁变薄、MVO心肌出现提示心肌损伤,射血分数降低、心房内径增大提示心脏收缩功能下降。但AMI患者多急性起病,缺乏发病及治疗前后对比。而心脏超声指标主观性较强,个体差异及临床表现极大,故难以作为临床试验终点指标进行分析。
对AMI心肌损伤的量化分析主要有N末端B型利钠肽原(NT-proBNP)、肌酸激酶同工酶(CK-MB)和心肌钙蛋白(cTn),该类生物标记物主要由细胞结构变形的受损心肌细胞产生,特异性较好,但在急性期过后快速下降,无法反应AMI免疫药物的远期心脏保护作用。
对AMI患者炎症程度的量化分析主要有高敏C反应蛋白(hsCRP),血清淀粉样蛋白(SAA),纤维蛋白原(Fb)等急性期蛋白和IL-6,TNF-α等细胞因子。由于急性期蛋白依赖心肌损伤后生成的细胞因子入血促进肝脏生成,故现有炎症相关AMI指标存在一定滞后性。虽然通过炎症反应程度间接判断心肌损伤程度的方式在评估AMI免疫药物时可能受到干扰,但仍为目前最可靠的AMI治疗的检验学临床指标。
其他扩展研究指标包括增量 PCAT、升主动脉最大TBR值、IL-8、MCP-1、sICAM、sVCAM等,这些指标反映了AMI在血管炎症和免疫细胞表型中的影响,诺和诺德在IL-6抑制剂Ziltivekimab开展的SPIDER试验中作为临床终点进行探索,但尚无相关数据和研究结果披露,有望成为后续AMI药物疗效的新评估方式。
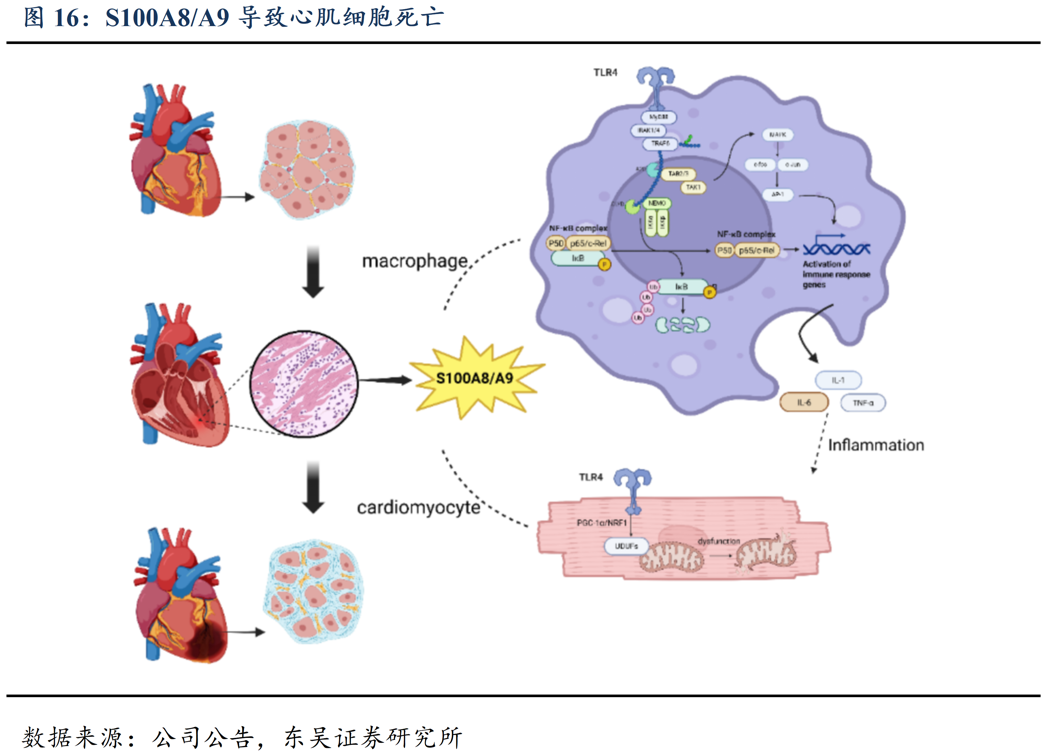
S100A8/A9具备成药靶点潜力。S100A8/A9是一种促炎因子,通常在正常心脏组织中表达较低,但在病理条件下(如心肌炎、缺血再灌注损伤、心衰等)其表达会显著上调,在损伤感知及心梗心衰启动中起关键作用,CXCR2+粒细胞分泌的S100A8/A9通过促进趋化因子的表达,招募更多炎症细胞,进一步加剧心肌损伤。主要在心肌细胞、心脏成纤维细胞、血管内皮细胞、中心粒细胞中出现高表达,并产生诱导线粒体功能异常,心肌细胞死亡、参与心脏纤维化、影响内皮细胞功能,参与血管炎症和通透性改变、招募更多免疫细胞释放炎症因子等危害。
阻断AMI炎症通路,差异性机制保护心肌。根据早研探索,S100A8/A9是一个行之有效的靶点,通过短期抑制阻断S100A8/A9,可有效阻断巨噬细胞TLR4/MAPK/NF-kB通路,减少IL-1/TNFa/IL-6等炎症因子分泌,减轻炎症风暴,防止心肌细胞里通过TLR4-UDUF诱导的线粒体功能异常,保护心肌细胞免于死亡,抑制心肌功能损伤。
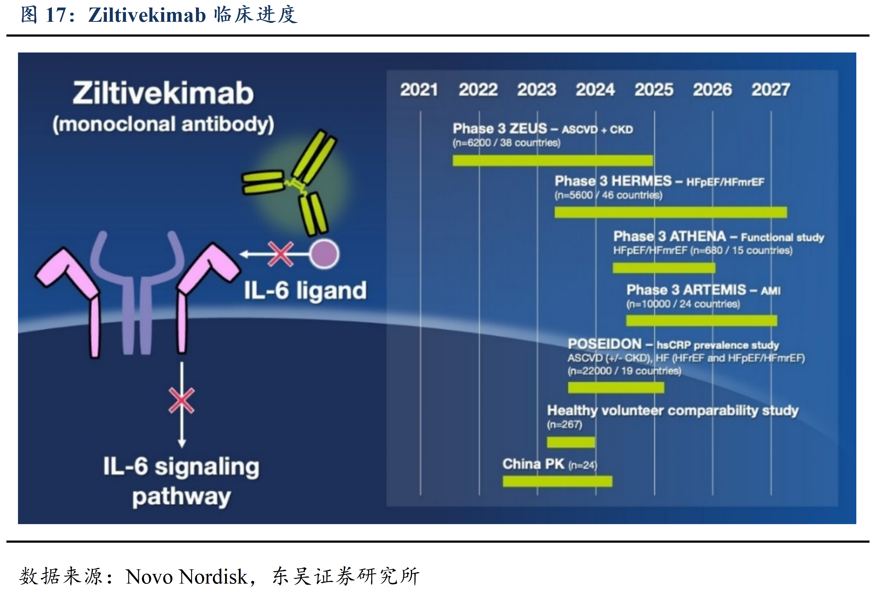
炎症反应相关通路药物在AMI新型药物研发中备受关注。临床阶段管线包括靶向S100A8/A9的SGC-001、靶向IL-6的诺和诺德拥有的Ziltivekimab(泽韦奇)和Pacibekitug。其中IL-6为S100A8/A9的下游分子,对S100A8/A9的靶向作用也会调控IL-6水平。Ziltivekimab于2024年8月启动多项国际多中心III期临床,其中AMI适应症选择了复发或合并糖尿病/卒中/慢性肾病的心肌梗死,从24个国家纳入10000名患者。研究主要终点为死亡/非致死性MI/非致死性卒中,除死亡率,就诊率,生存时间等指标外,选取了hs-CRP(高敏C反应蛋白)的变化作为重要的有效性指标。
已披露临床数据中,Ziltivekimab在II期临床试验RESCUE中降低了92%(对照组4%)的hsCRP ,Pacibekitug在II期临床试验TRANQUILITY中降低了86%(对照组15%)的hsCRP,两者均有10%的免疫相关不良反应。目前Ziltivekimab开展了ARTEMIS和ZEUS两项大型临床研究,分别专注于AMI的发生后疗效和发生前预防。其中ARTEMIS 正在为III期临床试验 STEMI 和 NSTEMI 分别在 36 小时和 72 小时内招募约 10,000 名患者,测试Ziltivekimab是否可以通过早期抑制 IL-6调节由心肌损伤引起的炎症反应。
2.1.3. SGC-001疗效显著,临床加速推进
SGC-001为全球首款FIC创新药,适用于急性心肌梗死。SGC001注射液是一款急救用单抗药物,首先开展的适应症为ST段抬高型前壁心肌梗死,由舜景医药孙志伟研发团队联合首都医科大学北京市心肺血管疾病研究所杜杰教授、李玉琳教授团队共同开发研制。
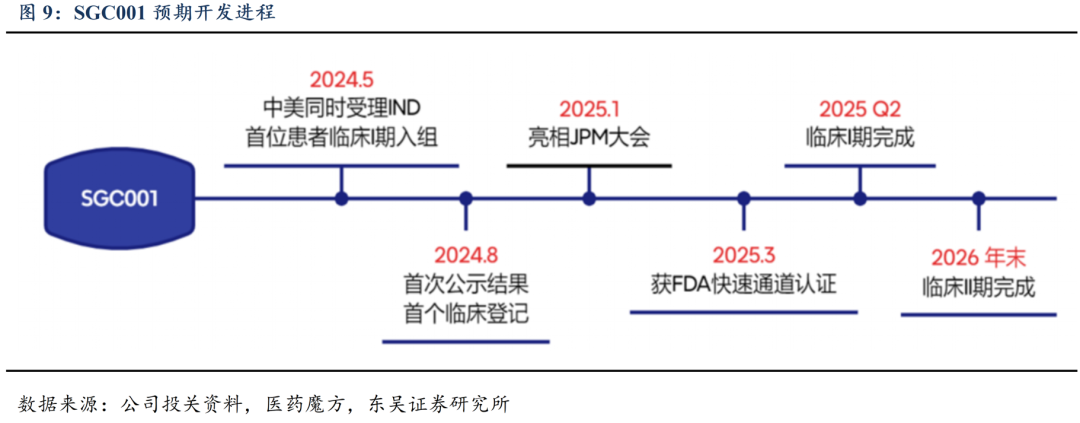
截至2025H1,SGC001的IND已先后获得FDA及国CDE的临床批准,并于2025年3月获得FDA授予的快速通道认证。舜景医药开展的创新药SGC001注射液分别在健康志愿者中和在前壁ST段抬高型心肌梗死患者中开展了2个I期研究:在健康志愿者中开展的Ia期临床研究已顺利完成;在前壁ST段抬高型心肌梗死患者中开展的Ib期临床研究于2024年11月27日获得组长单位哈尔滨医科大学第二附属医院伦理委员会批准,2025年1月首例受试者成功入组,于2025年7月完成所有受试者的临床观察,并于8月27日完成临床研究的揭盲。

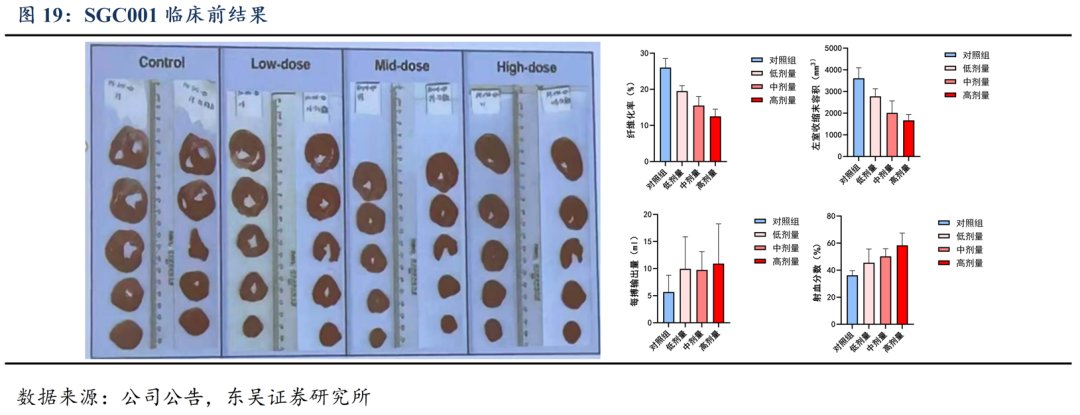
SGC-001临床前疗效理想,病理学证据明确。通过特异性结合并阻断S100A8/A9,可以抑制免疫细胞的炎症反应,并具有抗细胞凋亡的作用。在人源化全梗小鼠模型中,SGC-001显著降低了死亡率和心梗体积,改善了心脏功能,减轻了心肌病变,且与剂量呈明确的量效关系。在全梗恒河猴模型中,杜吉普单抗在低、中、高剂量下单次静脉给药,能够显著减轻心肌组织病变,降低心肌梗死体积并改善心功能。杜吉普单抗分别低、中、高剂量下单次静脉给药可以显著增加心梗恒河猴的心脏血流供应,并减轻心肌组织病变程度,其中降低心肌梗死体积均值分别减少23%、43%、53%,改善心功能射血分数分别提升了55%、141%、175%。提示SGC-001疗效理想,具有优良的成药特性。
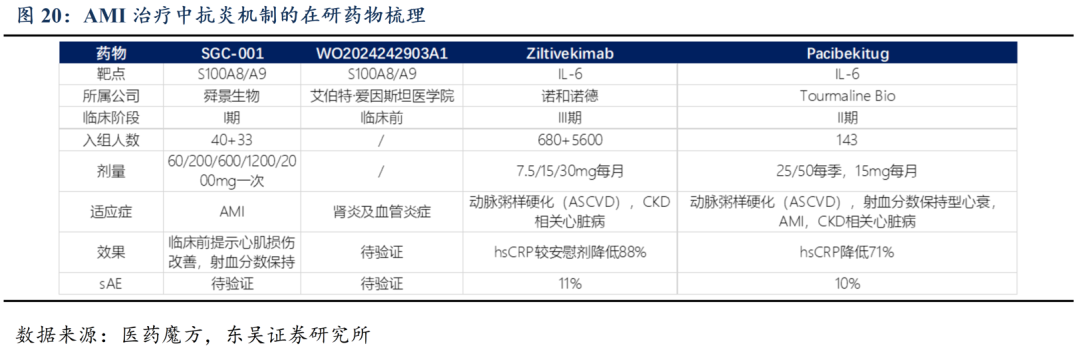
临床竞争格局领先。针对AMI疾病,暂无相关抗体药物进入临床研究阶段及审批上市。同靶点产品只有艾伯特・爱因斯坦医学院小分子在研药物WO2024242903A1与SGC-001的作用靶点相同,但目前主要拓展白血病、骨髓增生异常综合征与自身免疫性疾病适应症,目前进入临床前阶段,并于2024年11月28日公开专利。同赛道产品则包括靶向IL-6的诺和诺德拥有的Ziltivekimab和Tourmaline拥有的Pacibekitug。其靶点和SGC-001存在差异性,主要适应症为肾炎及血管炎症,于AMI领域的治疗潜力有待验证。公司产品临床前研究提示心肌保护明确,专注于AMI赛道,竞争力较强。
SGC-001有望填补AMI抗炎治疗领域空白。随着现代医学对AMI认知的加深,炎症和心肌保护在AMI治疗中的重要意义得以揭示,然而目前市场上缺乏相关治疗药物及相关适应症的拓展。SGC-001只要能够成药,则可以加入目前的各类AMI诊疗流程中,均存在预后改善,市场空间广阔。
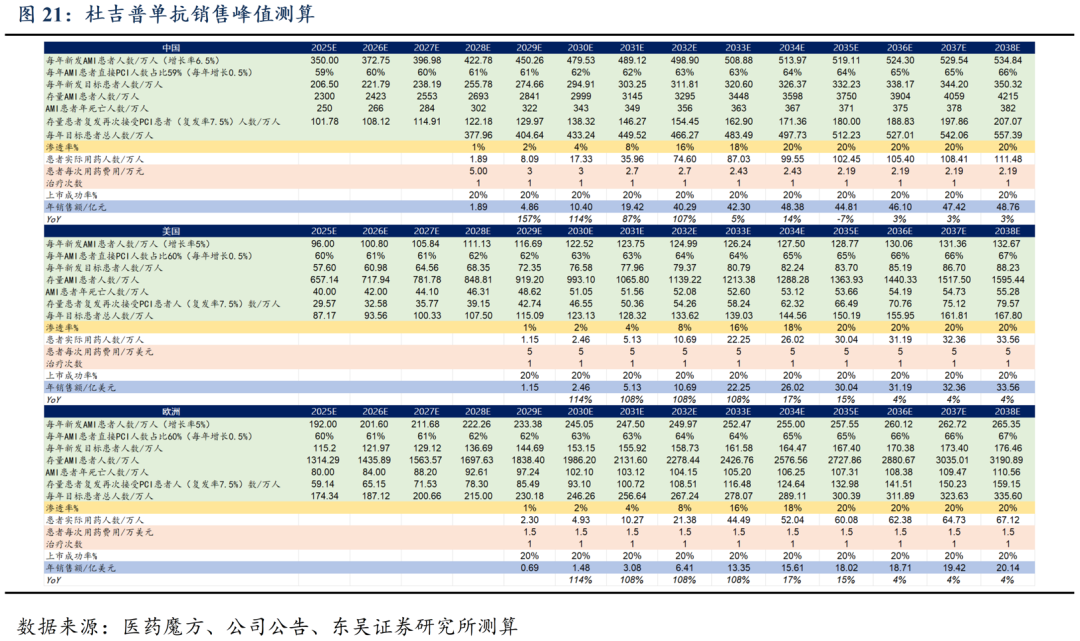
SGC-001销售峰值预测:1)患者数量:假定我国2025年新发AMI患者人数350万人,2030年新发480万人;美国/欧洲2025年新发AMI患者人数96/192万人,2030年新发123/245万人。2)药物降价幅度:假定国内患者用药费用5万元,后每两年医保降价;美国患者用药费用5万美元、欧洲患者用药费用1.5万美元。3)渗透率假设:传统再灌注疗法有限,杜吉普单抗的竞争格局良好,假设峰值渗透率为20%。基于上述假设,杜吉普单抗国内销售峰值我们预计于2034年达到48亿元(考虑风险折价)、欧美销售峰值于2038年达到54亿美元(考虑风险折价)。
2.2. 其他创新抗体药:SGT003和AA001
公司抗体平台建设初见成果,在肿瘤、神经、心血管领域均有靶点发现和管线产出。旗下公司舜景医药及智源生物除心血管领域重磅分子SGC001外,还有肿瘤领域靶向Tregs细胞的双抗药物SGT003和神经领域靶向Aβ蛋白的单抗药物AA001。公司创新抗体产品均使用独家发现的最新靶点,和市场上其余产品形成差异化,在同赛道药物中规避了机制同质化的竞争。
2.2.1. SGT003:靶向肿瘤免疫,临床前效果理想
舜景医药研发的双特异性抗体SGT003靶向肿瘤微环境中免疫抑制的Tregs细胞,能够显著减少Tregs细胞和肿瘤相关巨噬细胞的数量,利于清除肿瘤细胞,目前已进入临床前阶段。在第43届摩根大通医疗健康年会上,舜景医药发布了抗肿瘤核心管线SGT003项目进展数据。SGT003具有更强的肿瘤抑制效果、更高的安全性、可以诱导肿瘤免疫记忆。临床前研究数据显示,SGT003可显著减少Tregs和TAMs的数量。在更低的剂量作用下,SGT003对比已上市抗PD-1单抗和抗CTLA-4单抗的抑制肿瘤效果更显著,且不刺激TNF-α等因子释放,安全性大幅提高,展现出优秀的肿瘤治疗优势。动物实验显示SGT003治疗后动物机体可获得抗肿瘤免疫记忆,能够有效预防肿瘤的复发。SGT003有潜力成为更有效、更安全的新一代肿瘤免疫治疗一线基石药物。
2.2.2. AA001:直面AD挑战,新分子未来可期
阿尔茨海默症(AD)发现以来,就因其患病人群广,生活质量影响大,致病机制不明确,治疗效果不理想而成为全球药品研发的一大挑战。据《柳叶刀》报告,预计到2050年,全球痴呆症人数将由目前的5700万增加至1.53亿。而阿尔茨海默病正是痴呆症的主要类型。而AD赛道药物研发困难,失败的临床管线超过300种。传统的AD治疗药物如多奈哌齐、美金刚、石杉碱甲等神经递质调节、抗精神病、抗炎药物仅能改善AD症状,无法诊断AD病因进行治疗延缓疾病进展。
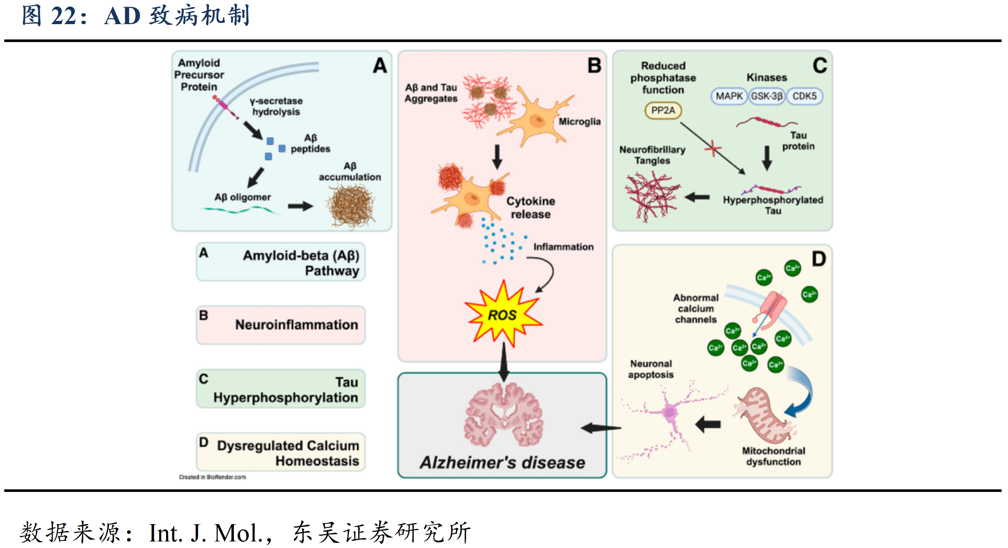
目前AD药物研发主要基于β-淀粉样蛋白(Aβ)学说和Tau学说,其中以Aβ学说目前成药效果最为理想。该学说认为,AD的发生和人脑神经细胞中蛋白质的错误折叠相关,错误折叠的Aβ会形成可溶性寡聚体及不溶性沉积斑块,产生神经毒性,导致突触功能损害和神经退行性变。对该过程的干预被证实可以减缓AD过程中的认知衰退。
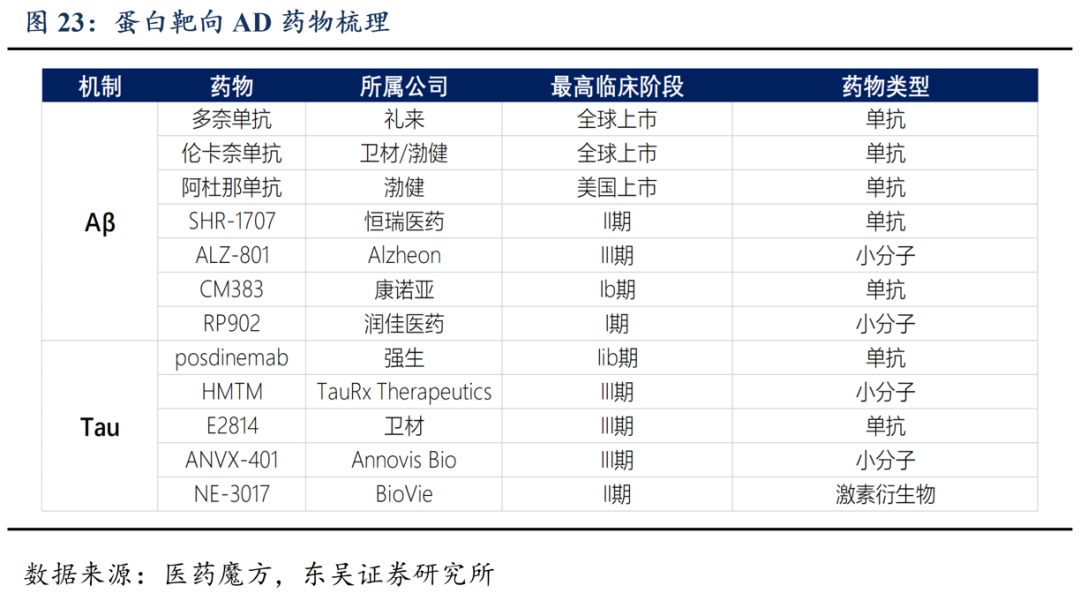
智源生物所研发的AA001创新药以anti-Aβ单抗机制来治疗阿兹海默病与轻度认知障碍,靶点为amyloid beta(Aβ),于2025年11月20日进入申报临床阶段,于2025年2月获批。智源生物刘瑞田教授研发团队通过十余年的探索,发现了阿尔茨海默病抗体药物介导神经突触过度丢失是导致免疫治疗失败的原因,提出采用无效应片段(Fc段)或无效应功能的β-淀粉样蛋白(Aβ)抗体具有较好前景的AD治疗新策略,可以提高抗体药物的疗效,降低毒副作用。AA001单抗即是基于该策略开发的新一代AD治疗抗体创新药,将为热景生物创新药研究带来新的突破。
2.3.尧景基因:小核酸药物递送方案
尧景基因专注于小核酸药物领域。公司拥有AI新药发现和设计、肝内外靶向递送、化学修饰等核心自主知识产权技术平台。2023年之前,公司专注于肿瘤诊断和治疗、外泌体技术平台的开发和应用。作为糖链外泌体诊断与治疗全球开创者,公司拥有基于糖链外泌体捕获平台GlyExo-Capture的核心技术及专利。而后出于战略考虑,公司专攻小核酸药物领域,布局多个小核酸药物管线,并自主研发包括靶向肌肉、脂肪、心脏、肾脏和神经系统的STT平台技术和序列设计修饰、靶点评估的FIST平台技术。
小核酸药物(siRNA/ASO)正逐步从罕见病治疗扩展至心血管代谢和神经系统疾病领域,反映了心血管患者基数庞大且残余风险仍高的临床现状。其应用的核心难点在于递送系统。核酸药物研发中的主要挑战之一是大部分靶点(约80%)位于心、肝等常规递送器官之外,而现有脂质纳米颗粒(LNP)在递送精准性方面存在明显限制。当前大多数RNA疗法项目仍处于临床前阶段,仅部分进入临床试验。Biogen重新布局ASO,CRISPR扩展至RNAi,Novartis与礼来持续推进心血管RNA项目,显示出全球龙头药企正通过商务开发积极进入小核酸领域。今年多笔交易的首付款与总潜在收益创下纪录,如Ionis-Ono高达近9亿美元的合作,Arrowhead与Sarepta初始交易金额超过8亿美元,充分反映出优质RNA资产和siRNA开发平台在早期阶段已具显著市场价值。
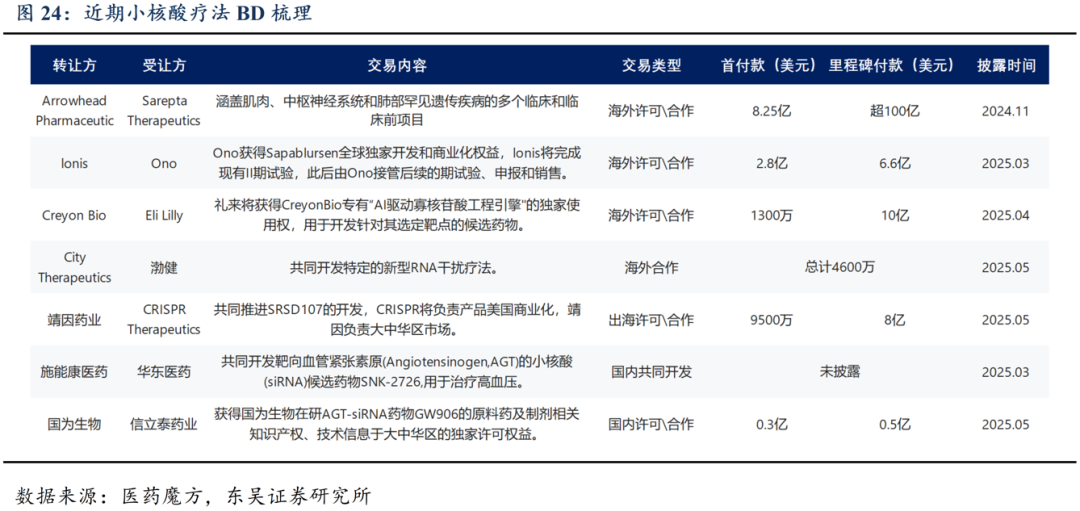
尧景基因通过FIST平台技术可预测siRNA序列的热力学稳定性、脱靶效应及体内代谢路径。创新的递送系统实现小核酸药物脑部、心肌、脂肪等多个肝外组织精准、高效的药物递送。目前已在小脑、肺、心、肝中验证了良好的递送效果,具备应用于肿瘤及罕见病等RNA药物领域的潜力,有望成为推动管线拓展的关键技术引擎。通过该平台得到了肥胖症药物Myostatin抑制剂和基于首个心肌细胞膜表面特异性高表达快速内化受体开发的AOC药物。大幅压缩了筛选时间,提高临床成药率及靶向递送效果。心脏siRNA偶联药物小鼠实验能够达到>95%的心脏敲低效果(1-3mg/kg),持续时间超过60天,与肝靶向标杆L96持平。NASH的siRNA药物在体外实验中抑制靶基因表达效率达92%,均高于同赛道产品水平。截至2025H1,公司已申请专利20项,提交4件专利优先权声明,并获得11项授权专利,其中包含1项PCT国际专利。

2.4. 禹景药业:聚焦活菌药物研发,AKK菌减重抗炎促代谢
热景生物在医疗美容与抗衰老领域的战略布局应势而起。作为生物技术消费品的倡导者和领航者,其孵化的北京禹景药业有限公司自主研发的Akkermansia muciniphilaYG2602(AKKYG2602)菌株,于2025年6月24日成功获得中国国家药品监督管理局化妆品新原料备案,成为全球首个获批用于化妆品的AKK菌原料。此前,禹景药业同源菌株AKKYG2645已于2025年1月28日通过美国FDA的GRAS(一般认为安全)认证。凭借这两项重要认证,禹景药业成为目前全球唯一同时拥有AKK菌化妆品新原料备案与AKK菌新食品原料认证的企业。
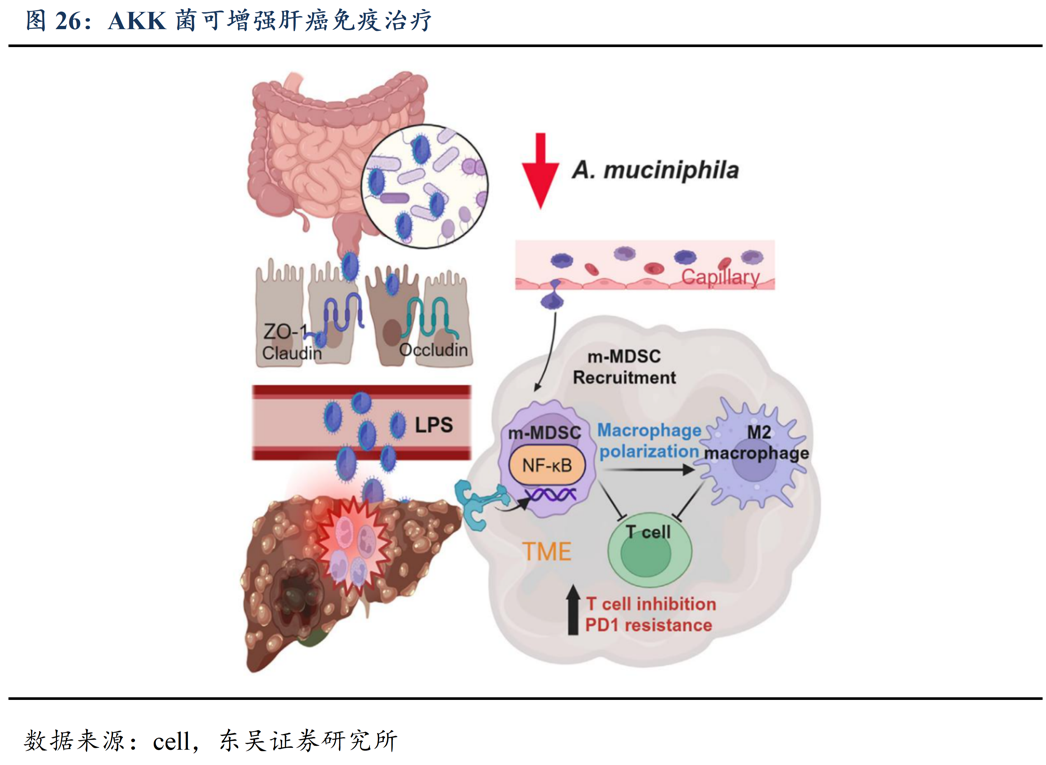
AKK菌是《Cell》《Nature》《Science》等顶级期刊持续关注的明星菌种,其独特的P9蛋白、Amuc_1100菌毛蛋白及胞外囊泡(EVs)等活性成分,在代谢疾病和神经退行性病变等领域展现出显著潜力,其能够刺激GLP1分泌,加速脂肪燃烧,调节肠道菌群,减少炎症反应,相比GLP1类药物减脂更温和-5.7%,体重-10.4%,空腹血糖-6.6%,脂肪代谢-12%,不良反应更小可长期使用,口服更方便。
禹景药业首次将AKK菌创新应用于美妆领域,成功开发出全球首款源自婴幼儿的化妆品级AKK菌株YG2602。研究揭示了该菌株通过四重协同通路赋能皮肤健康:1)抗衰老:抑制UVB诱导的活性氧(ROS)累积与细胞凋亡;2)屏障修复:显著上调胶原基因(COL17A1、COL1A1、COL3A1)及透明质酸合成酶基因(HAS1)表达,提升角质层含水量;3)抗炎舒缓:有效阻断LPS-TLR4炎症通路,抑制巨噬细胞系Raw264.7的炎症因子释放;4)抑制黑色素生成:降低黑色素合成限速酶酪氨酸酶(TYR)及关键因子TRP-1的表达水平。
3. IVD业务贡献基本盘,构建全场景诊断市场的核心技术矩阵
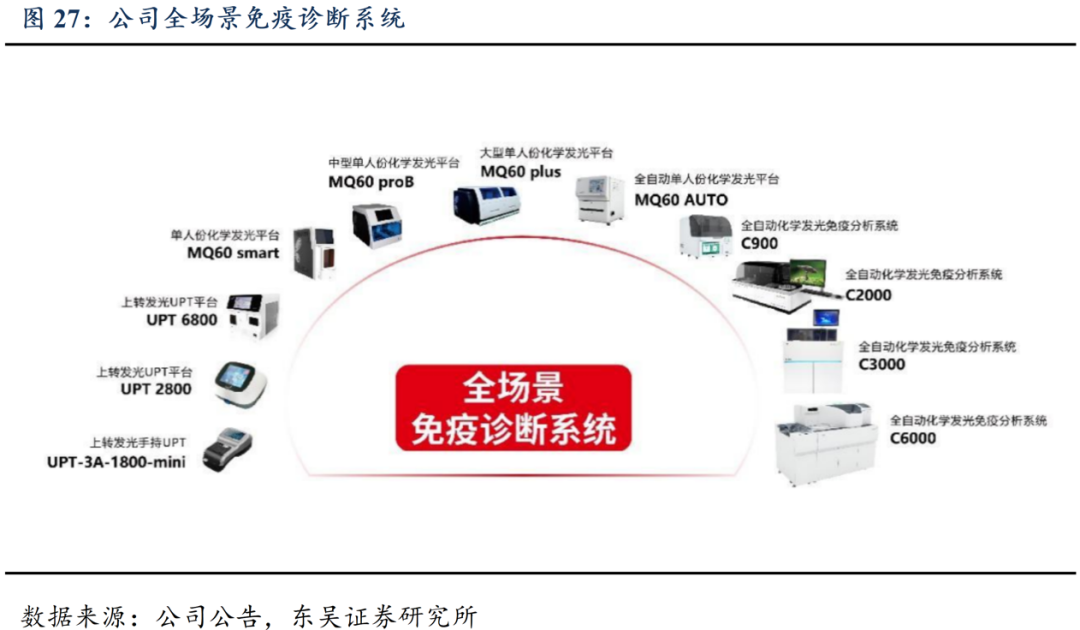
公司在体外诊断领域,一方面继续拓展原有核心技术平台的研发,扩展磁微粒化学发光、上转发光的检测试剂菜单;另一方面,积极拓展基于国际领先糖捕获技术的“国人肝健康工程”、“国人脑健康工程”和“国人癌症早诊早筛工程”为核心技术的三大“国人健康工程”,进一步拓宽、拓深体外诊断领域的核心战略布局;经过多年发展,构建了噬菌体大容量全合成人抗体制备技术平台、糖捕获技术平台、磁微粒化学发光技术平台、上转发光技术平台等多项核心技术平台,拥有多项前沿创新技术和创新产品,开发了一系列的体外诊断试剂及仪器,可应用于全场景的免疫诊断。
3.1. 产品新布局全面,涵盖大发光、小发光等技术
公司为业内为数不多的产品涵盖全场景应用的供应商之一。通过持续多年研发投入,公司掌握了单人份化学发光、全自动化学发光等核心技术,已获得II类和III类医疗器械注册证书127项(试剂116项,仪器11项),构建起可满足不同终端用户需求的全场景免疫诊断平台。截至25H1,C2000、C3000和C6000等C系列大型全自动化学发光仪器已实现装机1065余台,25H1新增装机175余台;公司单人份化学发光免疫分析仪(MQ系列)已顺利完成装机超14848个测试单元,25H1净新增测试单元948个。
磁微粒化学发光免疫分析法是将化学发光分析方法、磁性分离技术和酶免疫分析手段三者结合起来的一种新的分析方法。它利用了化学发光分析方法的高灵敏度,磁性分离方法的快速、易自动化及酶免疫分析方法较高的特异性等特点,可对小容量样本进行高精确度和高准确性的测定。与传统化学发光技术相比,磁微粒化学发光技术具有更低的背景噪声和更高的检测效率,尤其在癌症标志物检测中展现了显著优势。公司磁微粒化学发光法收入由2021年的1.44亿元增长至2024年的4.04亿元,2025H1为1.56亿元,同比下降22%。
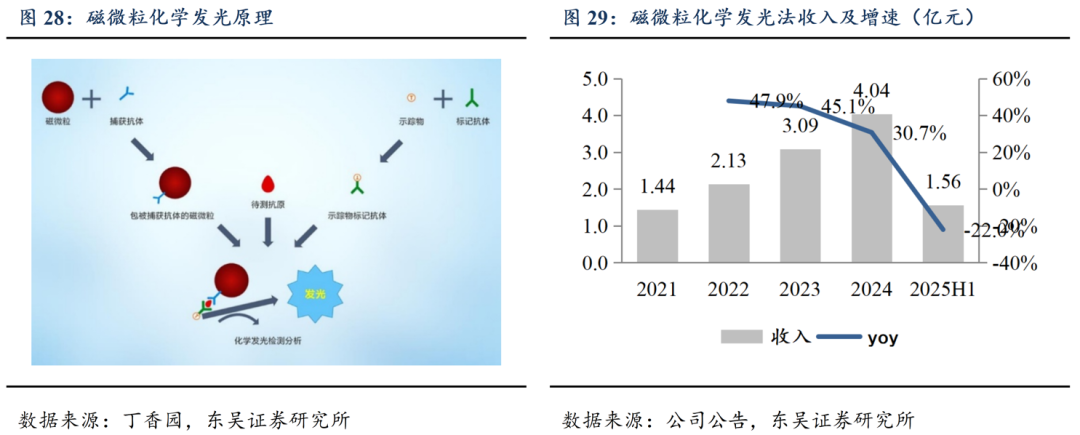
小型化学发光(小发光)和大型化学发光(大发光)是磁微粒化学发光技术的重要应用形式,二者的技术特点和市场定位存在显著差异。小型化学发光具有试剂独立包装、无样本量限制、随到随测、无需耗材等优势,特别适合基层医疗机构和特色临床科室使用,这些机构通常缺乏高端检测设备和技术人员,因此试剂独立包装和随到随测的特点成为关键优势。其仪器设计灵活,测试单元可自由组合,且维修保养简单,故障率低,能够满足基层医疗机构对快速、精准检测的需求;大型化学发光通常用于高通量、高效率的检测场景,如大型综合医院和第三方检测中心,这些机构需要高通量和高灵敏度的检测设备,以应对复杂疾病(如肿瘤、心脑血管疾病)的诊疗需求。通过提供全自动化学发光平台(如C2000、C3000系列),可以满足高端市场对高效、精准检测的追求。
受IVD行业集采等政策影响,短期国内价格下降及需求减少,25H1大发光及小发光增速下滑。2025H1,大发光平台(C2000、C3000等C系列试剂及仪器)实现营业收入7499.14万元,同比下滑1.97%;小发光平台(MQ60系列单人份试剂及仪器)实现营业收入8106.57万元,同比下滑34.43%。
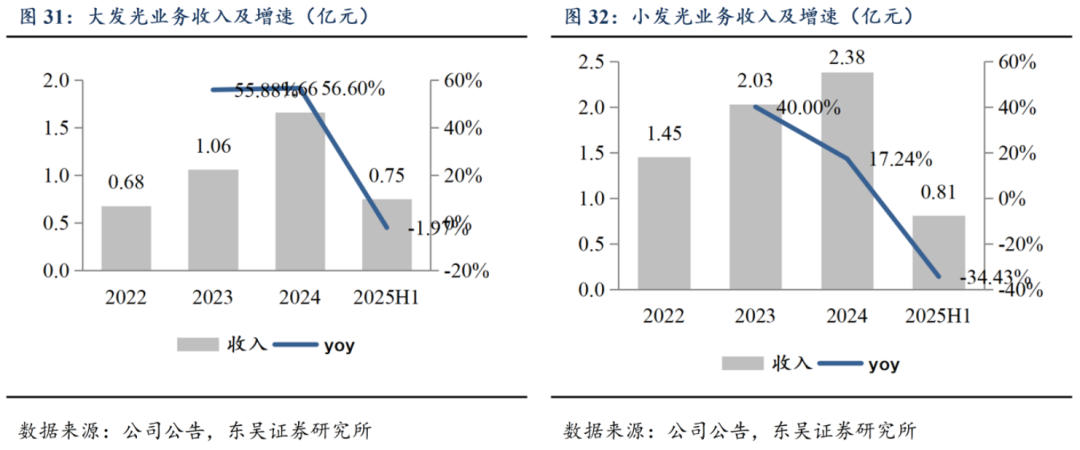
在目标市场方面,小型化学发光技术完美契合基层医疗机构的需求。根据国家卫健委统计,2023年我国基层医疗卫生机构数量达101.6万,包括社区卫生服务中心(站)、乡镇卫生院和村卫生室等。政策对基层医疗机构的支持为小型化学发光提供了广阔的市场空间。例如,2023年《关于进一步完善医疗卫生服务体系的意见》强调加强县级医院和基层医疗机构的检验能力建设。此外,随着人口老龄化和慢性病发病率的上升,基层医疗机构对快速检测的需求将进一步增长。
3.2. 糖捕获技术:助力“国人健康工程”发展
糖捕获技术是糖组学在临床诊断中的前沿应用,通过对特定糖链结构的高效识别和捕获,实现对疾病标志物的高灵敏度检测。相较于传统的蛋白质标志物检测,糖捕获技术具有更高的特异性和灵敏度。公司引入了纳米材料作为糖链捕获载体,利用纳米材料的高比表面积和功能化表面,显著提升了检测效率和准确性。
糖捕获技术的主要应用领域包括癌症早筛:在肝癌、胃癌、胰腺癌等多种癌症的早期筛查中。糖链与疾病状态密切相关,尤其是癌症和神经退行性疾病,可以成功应用于肝癌的早期筛查,通过检测甲胎蛋白异质体(AFP-L3%)等标志物实现对疾病相关标志物的精准检测,显著提高了早期肝癌的检出率。在阿尔茨海默病等神经退行性疾病的诊断中,糖捕获技术可用于检测与疾病相关的糖蛋白或外泌体,为疾病的早期干预提供依据。通过检测肝癌相关的糖链标志物,如AFP-L3%,结合其他指标构建风险预警模型,提升肝癌筛查的准确性。
公司糖捕获技术具备时效性及灵敏度。公司自主研发GlyExo-Capture?外泌体捕获技术,能够在短时间内高效提取富含特定糖链的外泌体,且操作简便,适用于临床应用;公司推出的外泌体microRNA全自动检测仪(EXO-01),实现了外泌体提取和检测的自动化,提高了检测效率和一致性;公司结合糖捕获技术获得的生物标志物数据,通过大数据分析和机器学习方法,建立疾病风险预测模型,如C-GALAD II肝癌风险预警模型。
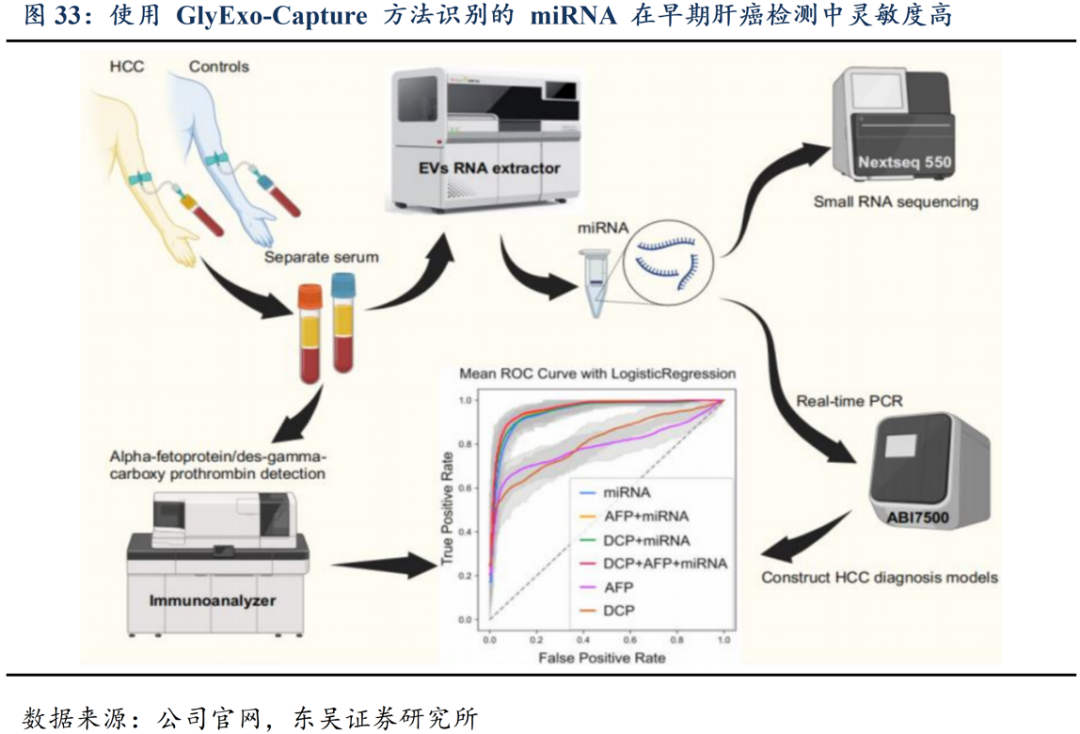
公司基于国际领先并具有核心自主知识产权的糖捕获技术平台,深耕液体活检的糖捕获检测技术,完成在糖链异常蛋白捕获检测技术、糖链外泌体捕获及外泌体核酸和蛋白检测技术的重大成果突破和战略布局,积极拓展公司在“国人肝健康工程”、“国人脑健康工程”和“国人癌症早诊早筛工程”为核心的三大“国人健康工程”的前沿技术布局。我国乙肝病毒携带者基数达8,600万(2024年《中国肝病防治白皮书》),肝癌高危人群二级预防依从性提升至31.5%,推动肝癌三联检(AFP/AFP-L3%/DCP)市场扩容。按高危人群年检测2次、单次检测费用约300元计算,肝癌早筛市场规模超百亿元。公司依托糖捕获技术实现肝癌三联检灵敏度突破92%(传统方法<70%),产品已覆盖全国百余家三甲医院,渗透率较2023年大幅提升。
3.3. 前沿技术平台业内领先
除磁微粒化学发光技术,糖捕获技术外,公司的噬菌体大容量全合成人抗体库制备技术和全场景化学发光仪器平台也处于行业前沿,共同构成公司IVD领域技术优势的四大前沿技术。
噬菌体大容量全合成人抗体库制备技术是现代抗体工程领域的前沿技术,公司通过全合成设计和基因工程技术构建了容量高达1010的抗体库。该技术的创新性在于利用计算机辅助设计构建高度多样化的抗体基因库,并通过噬菌体展示平台高效筛选出高亲和力、高特异性的抗体。相较于传统抗体库,全合成设计避免了免疫原性问题,显著提升了抗体的临床适用性。
全场景化学发光仪器平台是体外诊断仪器领域的前沿技术,热景生物通过模块化设计和智能化控制,实现了仪器在不同应用场景中的灵活适配。该平台的高通量检测能力和高度自动化设计显著提升了检测效率,通过优化硬件设计和软件算法,能够高效处理大规模样本并降低人工干预误差。此外,结合人工智能算法,该平台能够自动分析检测结果并提供诊断建议。
4. 盈利预测与估值
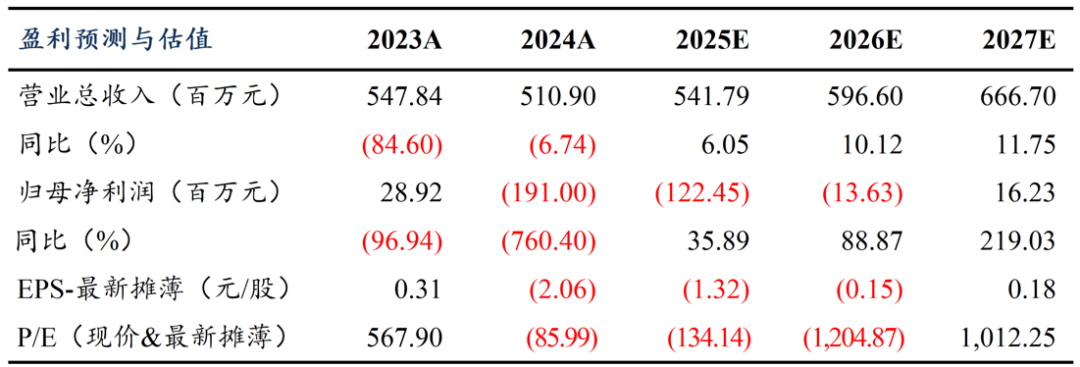
盈利预测及关键假设:
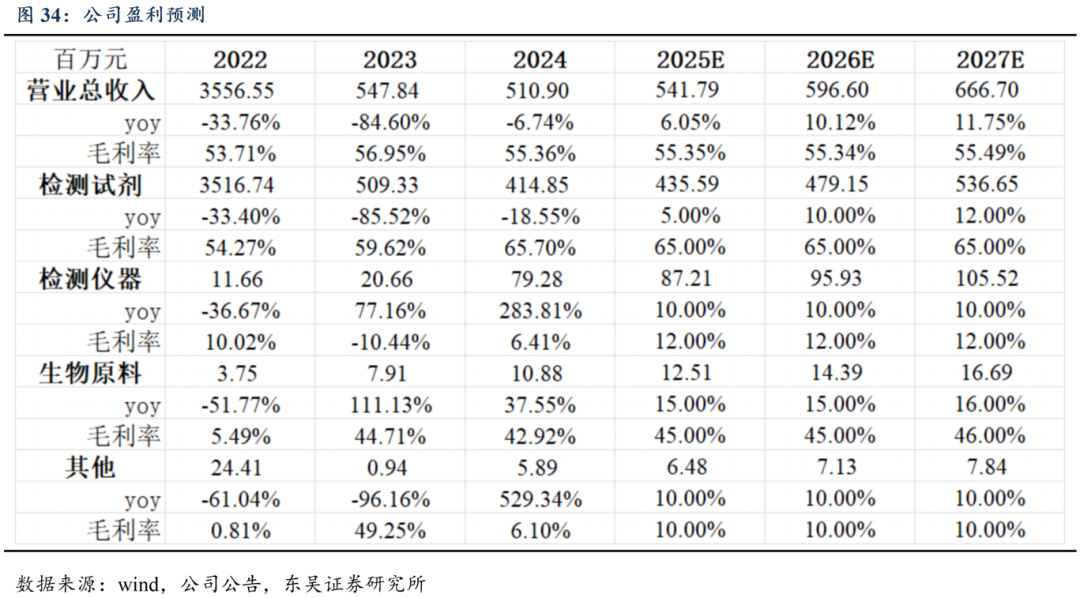
1、检测试剂:新冠影响基本出清,肝炎、心肌标志物等产品认可度逐步提升,需求持续释放,市占率有望提升。我们预计检测试剂2025-2027收入同比增长分别为5%、10%、12%,毛利率分别为65%、65%、65%。
2、检测仪器:随着试剂方案的不断丰富,对于检测仪器的需求也同步提升,而仪器市占率提升有望进一步带动试剂增长,公司通过多梯度产品矩阵实现免疫诊断全场景覆盖。我们预计检测仪器2025-2027年收入同比增长分别为10%、10%、10%,毛利率分别为12%、12%、12%。
3、生物原料:公司生物原料平台快速发展,认可度不断提高,且随着产能扩增毛利率有望进一步提升。我们预计生物原料2025-2027年收入同比增长分别为15%、15%、16%,毛利率分别为45%、45%、46%。
4、费用预测:我们预计2025-2027年销售费用率为38%、26%、24%;管理费用率为20%、17%、14%;研发费用率为20%、20%、20%。
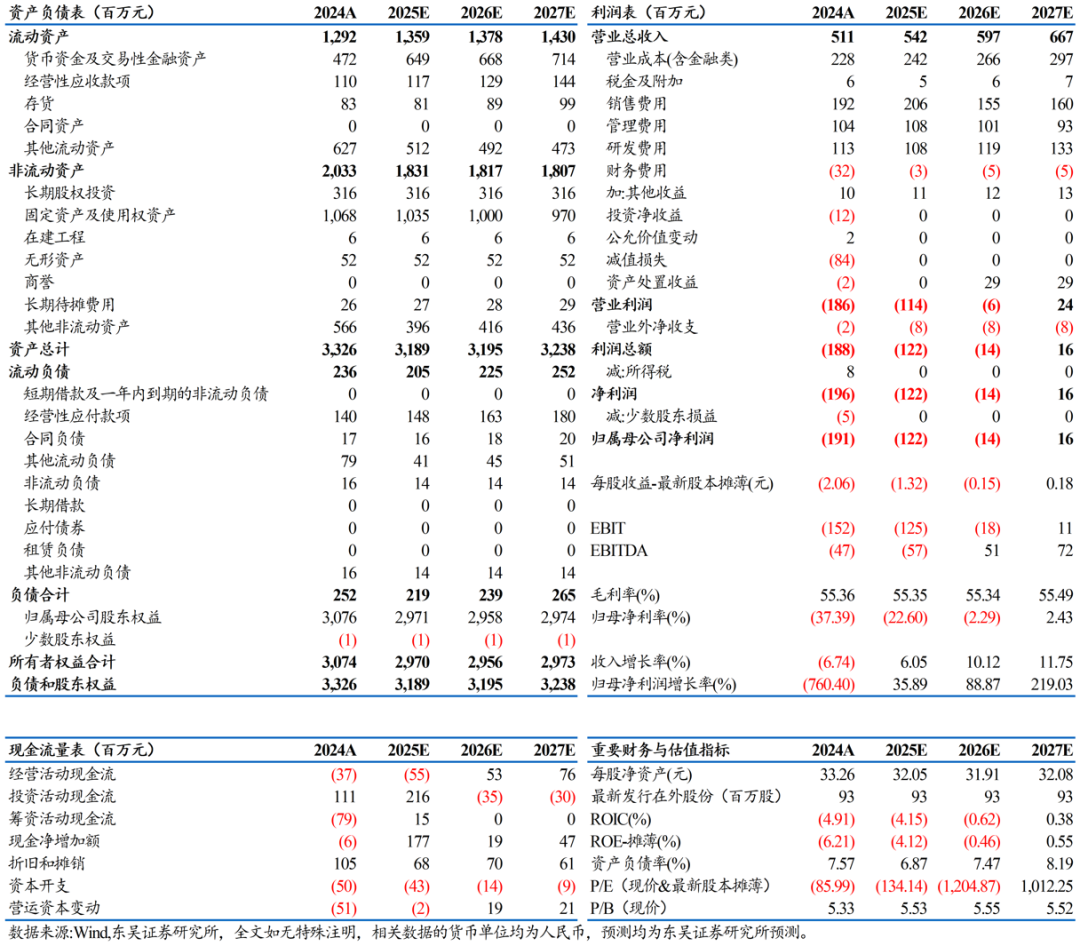
综上,我们预计公司 2025-2027 年收入分别为5.42、5.97、6.67亿元,归母净利润分别为-1.22、-0.13、0.17亿元。考虑公司IVD主业销售稳定,未来逐步贡献利润,在研创新药贡献较大市值弹性,我们选取分部估值法。
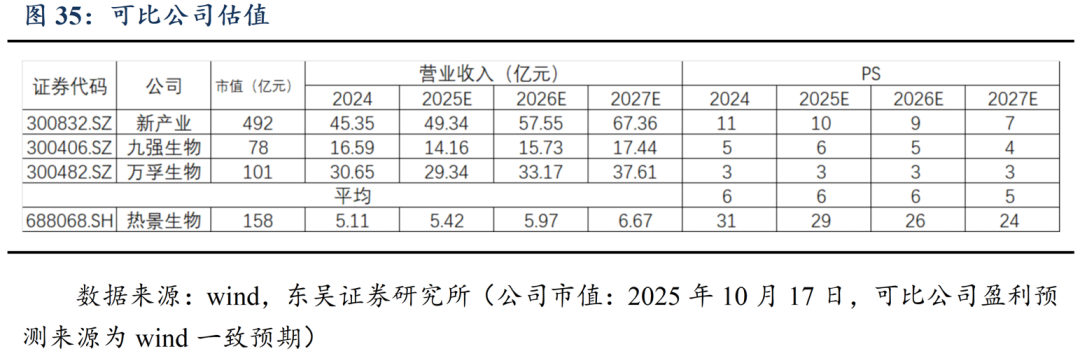
1)主业IVD部分:我们选取业务模式相近的IVD公司新产业、九强生物、万孚生物作为可比公司,可比公司2026年平均PS为6倍,热景生物2026年收入5.97亿元,对应市值36亿。
2)创新药部分:SGC001国内销售峰值48亿元,3倍PS对应144亿市值;欧美销售峰值54亿美金,按10%分成及10倍PE折现后贡献378亿;公司持股其45.58%权益,故SGC001合计贡献238亿元。
3)AKK菌:保健品国内我们预计10亿销售峰值,3倍PS及58%持股比例对应市值17亿。
4)小核酸平台:我们预计50亿美金峰值,1倍PS及45%股权贡献158亿。
5)I/O双抗SGC003风险调整后我们预计10亿美金峰值,1倍PS及45%股权贡献32亿。
综上,公司主业IVD、创新药部分、AKK菌及小核酸平台合计有望贡献480亿市值。考虑公司主业IVD业务贡献基本盘,参股公司创新药管线持续推进,核心产品SGC001为AMI领域FIC,逐步转型创新,首次覆盖,给予“买入”评级。
5. 风险提示
1、产品研发失败风险:公司核心管线SGC001及AA001存在研发失败风险,导致公司市场竞争力下滑。
2、销售不及预期风险:公司IVD产品及未来拟获批创新药产品销售若不及预期,则会影响公司整体收入。
3、集采风险:公司主业IVD产品可能受集采影响,导致出厂价波动与丢标风险。